WikiDer > 3 топ элементі
| 3 топ периодтық жүйеде | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| ↓ Кезең | |||||||||
| 4 | Скандий (Sc) 21 Өтпелі металл | ||||||||
| 5 | Итрий (Y) 39 Өтпелі металл | ||||||||
| 6 | Лантан (Ла *) 57 Лантаноид | ||||||||
| 6 | Лютеций (Лу *) 71 Лантаноид | ||||||||
| 7 | Актиниум (Ac *) 89 Актинид | ||||||||
| 7 | Lawrencium (Lr *) 103 Актинид | ||||||||
* Элементтері лантан (La) және актиний (Ac) немесе элементтер лютеий (Лу) және lawrencium (Lr) 3-топта даулы. Қараңыз 3 топтың құрамы. | |||||||||
Аңыз
| |||||||||
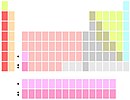
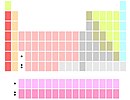
3 топ Бұл топ туралы элементтер ішінде периодтық кесте. Бұл топ, басқалары сияқты d-блок төрт элементтен тұруы керек, бірақ топқа қандай элементтер кіретіні келісілмеген. Скандий (Sc) және иттрий (Y) әрқашан қосылады; итрий астындағы кеңістікті не алады лантан (La) және актиний (Ac) немесе лютеий (Лу) және lawrencium (Lr), бұрынғы опция кең таралған. Көбінесе топ 32 элементке дейін кеңейтілуі керек деп саналады (барлық лантаноидтар және актинидтер қосылды) немесе La-Ac және Lu-Lr екеуін қосу үшін бифуркацияланған. Топта лантаноидтардың барлығы бар деп түсінгенде, ол оларды қосады сирек жер металдары. Итрий, және сирек кездесетін скандий кейде сирек кездесетін металдар болып саналады.
Үш топтың үш элементі табиғи түрде пайда болады: скандий, иттрий және лантан немесе лютеий. Лантан жалпы химиялық мінез-құлықтағы екі жеңіл мүше бастаған тенденцияны жалғастырады, ал лютеций иттрияға ұқсас. Лютециумды таңдау тенденцияға сәйкес келеді кезең 6 ауыспалы металдар өздерінің жоғарғы периодтық кестесінің көршілеріне ұқсас болып жүреді, лантанды таңдау тенденцияларға сәйкес келеді s-блок, 3 топ элементтері химиялық жағынан біршама ұқсас (олар сияқты) лантаноидтар және актинидтер жалпы алғанда, сондай-ақ 4 және 5 топтардың ауыр элементтері). Олардың барлығы стандартты жағдайларда күмістей ақ металдар. Төртінші элемент, актиний немесе луренций, тек радиоактивті болады изотоптар. Актиний, ол тек кездеседі іздер, а-мен трипозитивті ион түзетін металдар үшін химиялық мінез-құлық үрдісін жалғастырады асыл газ конфигурация; синтетикалық lawrencium есептеліп, ішінара лутетий мен иттрийге ұқсас екендігі көрсетілген. Әзірге ешқандай эксперименттер жүргізілген жоқ синтездеу келесі 3 топ элементі бола алатын кез келген элемент. Unbiunium (Ubu), егер оның алдында лантан мен актиний болса, 3-топ элементі деп санауға болады, жақын уақытта синтезделуі мүмкін, бұл қазіргі ең ауыр элементтен үш кеңістікте ғана, огангессон.
Тарих
1787 жылы шведтің штаттан тыс химигі Карл Аксель Аррениус швед ауылының маңынан ауыр қара тасты тапты Итерби, Швеция (бөлігі Стокгольм архипелагы).[1] Бұл жаңадан табылған элементі бар белгісіз минерал деп ойлау вольфрам,[2] ол оны атады итербит.[n 1] Фин ғалымы Йохан Гадолин жаңа оксидті анықтады немесе «жер«1789 жылы Аррениус үлгісінде және 1794 жылы өзінің аяқталған талдауын жариялады;[3] 1797 жылы жаңа оксид аталды итрия.[4] Француз ғалымынан кейінгі онжылдықта Антуан Лавуазье алғашқы заманауи анықтамасын жасады химиялық элементтер, Жерді элементтеріне дейін азайтуға болады деп сенді, яғни жаңа жердің ашылуы ішіндегі элементтің ашылуына тең болды, бұл жағдайда иттрий.[n 2] 20-шы жылдардың басына дейін элемент үшін «Yt» химиялық белгісі қолданылған, содан кейін «Y» жалпы қолданысқа ене бастаған.[5] Итрий металы алғаш рет 1828 жылы оқшауланған Фридрих Вёлер қыздырылған сусыз иттрий (III) хлорид бірге калий металды иттрий және калий хлориді.[6][7]
1869 жылы орыс химигі Дмитрий Менделеев өзінің итрийдің үстінде және астында элементтерге арналған бос орындары бар өзінің периодтық жүйесін жариялады.[8] Менделеев иттрияның жоғарғы көршісі туралы бірнеше болжам жасады, оны ол атады эка-бор. Швед химигі Ларс Фредрик Нильсон және оның тобы минералдардағы жетіспейтін элементті тапты эвсенит және гадолинит және 2 грамм дайындалған скандий (III) оксиді жоғары тазалық.[9][10] Ол оны скандий деп атады Латын Скандия «Скандинавия» деген мағынаны білдіреді. Элементтегі химиялық тәжірибелер мұны дәлелдеді Менделеевтің ұсыныстары дұрыс болды; табу мен сипаттаумен қатар галлий және германий бұл бүкіл периодтық жүйенің дұрыстығын дәлелдеді және мерзімді заң. Нильсон Менделеевтің болжамын білмеген сияқты, бірақ Теодор Клив үшін хат-хабарды танып, Менделеевке хабарлама жасады.[11] Металл скандийі алғаш рет 1937 жылы өндірілді электролиз а эвтектика қоспасы, 700-800 ° C, калий, литий, және скандий хлориді.[12]
1751 жылы швед минералогы Аксель Фредрик Кронштедт кезінде шахтадан ауыр минерал табылды Бастнас, кейінірек аталған церит. Отыз жылдан кейін он бес жасар бала Вильгельм Хизингер, шахтаға ие отбасынан, оның үлгісін жіберді Карл Шелеішінде жаңа элементтер таппаған. 1803 жылы Хизингер темір ұстасы болғаннан кейін, ол минералға оралды Джонс Якоб Берцелиус және олар атаған жаңа оксидті бөліп алды церия кейін карликовая планета Сериялар, екі жыл бұрын табылған.[13] Германияда бір уақытта Церия дербес оқшауланған Мартин Генрих Клапрот.[14] 1839-1843 жылдар аралығында церия оксидтер қоспасы ретінде швед хирургі мен химигі көрсеткен Карл Густаф МозандерБерзелиуспен бір үйде тұрған: ол өзі атаған тағы екі оксидті бөліп алды лантана және димия.[15] Ол үлгіні ішінара ыдыратты церий нитраты оны ауада қуырып, содан кейін алынған оксидті сұйылтылған күйде өңдеу арқылы азот қышқылы.[16] Лантанның қасиеттері церийден аз ғана ерекшеленетіндіктен және онымен бірге оның тұздарында пайда болғандықтан, ол оны Ежелгі грек λανθάνειν [лантанейн] (жарық жасырын жату).[14] Салыстырмалы түрде таза лантан металы алғаш рет 1923 жылы оқшауланған.[17]
Лутеций дербес болды табылды француз ғалымы 1907 ж Джордж Урбаин,[18] Австриялық минеролог барон Карл Ауэр фон Вельсбахжәне американдық химик Чарльз Джеймс[19] минералдағы қоспа ретінде итербиа, оны көптеген химиктер толығымен құрайтын деп ойлады итербиум. Вельсбах атауларды ұсынды кассиопеиум 71 элементі үшін (шоқжұлдыздан кейін Кассиопея) және альдебарани (жұлдыздан кейін Альдебаран) итербиумның жаңа атауы үшін, бірақ бұл атаулар туралы ұсыныстар қабылданбады, дегенмен көптеген неміс ғалымдары 1950-ші жылдары 71-ші элементті кассиопей деп атады. Урбаин есімдерді таңдады неоитербиум (Латын «жаңа итербиум» үшін) итербиум үшін және лютециум (латынша Лютециядан, Париж үшін) жаңа элемент үшін. Табудың басымдығы туралы дау екі мақалада жазылған, онда Урбаин мен фон Вельсбах бірін-бірі жариялаған зерттеулердің әсерінен жариялау нәтижелерінде айыптайды.[20][21] Атомдарды жаңа элементтерге жатқызуға жауапты атомдық масса жөніндегі комиссия 1909 жылы Урбаинға басымдық беріп, оның есімдерін ресми деп қабылдау арқылы дауды шешті. Бұл шешімнің айқын проблемасы Урбаин комиссияның төрт мүшесінің бірі болғандығы болды.[22] Лутецийдің итербийден бөлінуін алдымен Урбаин сипаттаған, сондықтан ат қою құрметі оған ие болды, бірақ неоитербиум ақырында итербиумға оралды және 1949 жылы 71 элементтің емлесі лютецийге өзгертілді.[23][24] Бір қызығы, басымдылық туралы даудан қарапайым болған Чарльз Джеймс басқаларға қарағанда әлдеқайда ауқымды жұмыс істеді және сол кездегі ең үлкен лютеций қорына ие болғаны сөзсіз.[25]
Андре-Луи Дебьер, француз химигі 1899 жылы актиниумның ашылғанын жариялады. Ол оны бөлді шайыр қалдықтар Мари және Пьер Кюри олар шығарғаннан кейін радий. 1899 жылы Дебьерн затты ұқсас деп сипаттады титан[26] және (1900 ж.) ұқсас торий.[27] Фридрих Оскар Гизель актиниумды өз бетінше 1902 ж. ашты[28] ұқсас зат ретінде лантан және оны 1904 жылы «эмания» деп атады.[29] Дебьерн анықтаған жартылай шығарылу кезеңін салыстырғаннан кейін,[30] Хариетт Брукс 1904 жылы және Отто Хан және Отто Сакур 1905 жылы жаңа элемент үшін Дебьерннің таңдаған атауы сақталды, өйткені оның химиялық құрамы әртүрлі болған кезде қайшы келетін химиялық қасиеттеріне қарамастан, старший болды.[31][32]

Лоуренций алғаш рет синтезделді Альберт Гиорсо және оның командасы 1961 жылы 14 ақпанда, Лоуренс радиациялық зертханасында (қазіргі кезде деп аталады) Лоуренс Беркли атындағы ұлттық зертхана) кезінде Калифорния университеті жылы Беркли, Калифорния, АҚШ. Lawrencium-дің алғашқы атомдары элементтің үш изотопынан тұратын үш миллиграмдық нысанды бомбалау арқылы пайда болды. калифорний бірге бор-10 және бор-11 ядролар ауыр ионды сызықтық үдеткіштен (HILAC).[33] The нуклид 257103 бастапқыда хабарланған, бірақ кейін ол қайта тағайындалды 258103. Калифорния университетінің командасы бұл атауды ұсынды lawrencium (кейін Эрнест О. Лоуренс, өнертапқыш циклотрон бөлшектер үдеткіші) және «Lw» белгісі,[33] жаңа элемент үшін, бірақ «Lw» қабылданбады, ал оның орнына «Lr» ресми түрде қабылданды. Ядролық-физиканы зерттеушілер Дубна, кеңес Одағы (қазір Ресей), 1967 жылы американдық ғалымдардың мәліметтерін растай алмағаны туралы хабарлады 257103.[34] Екі жыл бұрын Дубна командасы хабарлады 256103.[35] 1992 жылы IUPAC Транс-фермиумның жұмыс тобы 103-элементті ресми түрде мойындады, оның «Lr» белгісімен луренциум деп атауын растады және Дубна мен Берклидегі ядролық физика командаларын заңның бірлескен ашушылары ретінде атады.[36]
Егер лутетий мен лавренций 3-топ элементтері болып саналса, онда -дан экстраполяция Aufbau принципі топтағы келесі элемент 153 элемент, unpenttrium (Upt) болуы керек деп болжайды. Принцип бойынша, unpenttrium [Og] 8s электронды конфигурациясына ие болуы керек25г186f147д1[n 3] және 5g-ішкі қабықты толтыруды 138 элементте тоқтату керек. Алайда, 120-дан асатын элементтер Aufbau принципіне сәйкес тоқтайды деп болжануда: 7d-орбитальдар 137 элементте толтырыла бастайды деп есептеледі, ал 5g-қабықша тек элементте жабылады 144, кейін 7d-subhell толтыру басталады. Сондықтан, келесі 3-топ элементінің қай элемент болуы керектігін есептеу қиын.[37] Есептеулер бойынша, диспентентиум (Upp, элемент 155) келесі 3 топ элементі бола алады,[38] пепцептиум сияқты (Ups, элемент 157).[39] Егер лантан мен актиний 3 топтың элементтері болып саналса, онда 121 элемент, унбиуний (Убу), үшінші топтың бесінші элементі болуы керек. Элемент [Og] 8s электронды конфигурациясына есептелген28p1/21, заңсызға ұқсас аномальды р-электронмен.[37] 1977 жылы унбиуний синтезі сәтсіз аяқталды,[40] дегенмен оның белгілі элементтерге жақындығы және үдеткіш технологиясының жетістіктері оны жақын арада құруға мүмкіндік беруі мүмкін.[41][42] Басқа синтездеу эксперименттері жүргізілген жоқ.
Сипаттамалары
Химиялық
| З | Элемент | Электрондық конфигурация |
|---|---|---|
| 21 | скандий | 2, 8, 9, 2 |
| 39 | иттрий | 2, 8, 18, 9, 2 |
| 57 | лантан | 2, 8, 18, 18, 9, 2 |
| 71 | лютеий | 2, 8, 18, 32, 9, 2 |
| 89 | актиний | 2, 8, 18, 32, 18, 9, 2 |
| 103 | lawrencium | 2, 8, 18, 32, 32, 8, 3 |
Басқа топтар сияқты, бұл отбасы мүшелері де электронды конфигурациясының заңдылықтарын, әсіресе сыртқы қабықшаларын көрсетеді, нәтижесінде химиялық мінез-құлық үрдістері пайда болады. Алайда, лурренций - бұл ерекше жағдай, өйткені оның соңғы электроны 7-ге көшеді1/2 байланысты қабық релятивистік эффекттер.[43][44]
Химияның көп бөлігі топтың алғашқы үш мүшесінде ғана байқалды; актиниумның және әсіресе луренцийдің химиялық қасиеттері жақсы сипатталмаған. Топтың қалған элементтері (скандий, иттрий, лутетий) - балқу температурасы жоғары реактивті металдар (сәйкесінше 1541 ° C, 1526 ° C, 1652 ° C). Әдетте олар скандий болса да, +3 тотығу дәрежесіне дейін тотығады,[45] иттрий[46][47] және лантан[17] төменгі тотығу дәрежелерін құра алады. Элементтердің реактивтілігі, әсіресе иттрий тұрақты оксид қабаты пайда болуына байланысты әрдайым айқын бола бермейді, бұл әрі қарайғы реакцияларға жол бермейді. Скандий (III) оксиді, иттрий (III) оксиді, лантан (III) оксиді және люций (III) оксиді ақ температурада балқитын қатты заттар. Итрий (III) оксиді және лютеий (III) оксиді әлсіз негіздік сипатта болады, ал скандий (III) оксиді амфотериялық.[48] Лантан (III) оксиді қатты негізгі.[дәйексөз қажет]
Физикалық
Электронды конфигурациясы бар трипозитивті иондарды көрсететін элементтер (скандий, иттрий, лантан, актиний) физикалық қасиеттерінде қаттылық сияқты айқын сызықтық тенденцияны көрсетеді. Сонымен қатар, егер 3 топ лютециймен және луренцеймен жалғасатын болса, онда тенденциялар басқа d-блок топтарының бағыттарын ұстанып, толтырылған f-қабықшаның ядроға қосылуын көрсетеді. Мысалы, скандий мен иттрий - екеуі де жұмсақ металдар. Лантан жұмсақ; бұл элементтердің барлығында ядро зарядтарымен салыстырғанда ядродан едәуір алыстағы электрондары бар. Байланысты лантанидтің жиырылуы, лантанид сериясындағы соңғы лютеий, атом радиусы едәуір кіші және ядро заряды жоғары,[49] осылайша электрондарды атомнан түзуге айналдырады металл байланысы неғұрлым қиын, осылайша металды қатаңдатады. Алайда, лютеий алдыңғы элементтерге бірнеше басқа қасиеттерге сәйкес келеді, мысалы балқу[50] және қайнау температурасы.[51] Лавренций туралы өте аз мәлімет және оның физикалық қасиеттерінің ешқайсысы расталмаған.[52][53]
| Аты-жөні | Скандий | Итрий | Лантан | Лютеций | Актиниум | Lawrencium |
|---|---|---|---|---|---|---|
| Еру нүктесі[50] | 1814 К, 1541 ° С | 1799 K, 1526 ° C | 1193 K, 920 ° C | 1925 K, 1652 ° C | 1323 K, 1050 ° C | ? 1900 К,? 1627 ° C |
| Қайнау температурасы[51] | 3109 K, 2836 ° C | 3609 K, 3336 ° C | 3737 K, 3464 ° C | 3675 К, 3402 ° С | 3471 K, 3198 ° C | ? |
| Тығыздығы | 2,99 г · см−3[55] | 4,47 г · см−3[56] | 6,162 г · см−3 | 9,84 г · см−3 | 10 г · см−3 | ? 16 г · см−3 |
| Сыртқы түрі | күміс металл | күміс ақ | сұр | күміс сұр | күміс | ? |
| Атом радиусы[49] | Кешкі 162 | Кешкі 180 | Кешкі 187 | Кешкі 174 | 215 сағат | ? |
3 топтың құрамы
Скандий мен иттрий әрқашан 3-топтағы алғашқы екі элемент болғанымен, келесі екі элементтің сәйкестігі толық шешілмеген. Олар әдетте лантан және актинийжәне аз лютеий және lawrencium. Екі нұсқа лантаноидтарды периодтық жүйеге орналастырудағы тарихи қиындықтардан және f блок элементтері басталады және аяқталады.[57]
Лантаноидтардың периодтық жүйенің негізгі бөлігінен бөлінуі чех химигіне жатқызылған Богуслав Браунер ол 1902 жылы олардың барлығын («Се т.б.») цирконийден төмен, 4-топтағы бір позицияға бөлді. Бұл жүйені Күн жүйесіндегі бір орбита алып жатқан астероидтарға ұқсас «астероид гипотезасы» деп атады. Осы уақытқа дейін лантаноидтар негізінен 8-бағаннан тұратын периодтық жүйенің I-VIII топтарына орналастырылды (және сәтсіз). Браунердің 1902 жылғы орналасуының предшественниктері 1895 жылдың өзінде-ақ жазылғанымен, ол 1881 жылы Менделеевке жазған хатында «астероидтар химиясы» туралы айтқаны белгілі. Басқа авторлар барлық лантаноидтарды 3 топқа, 3 және 4 топтарға немесе 2, 3 және 4 топтарға тағайындады. 1922 ж. Нильс Бор s- және d-блоктарының арасына лантаноидтарды орналастыру арқылы бөлу процесін жалғастырды. 1949 жылы Гленн Т. (қайта) лантаноидтар мен актинидтер түсіндірме ретінде пайда болатын, қазіргі кезде кең таралған периодтық жүйенің формасын енгізді. Алғаш рет Seaborg өз кестесін 1944 жылы жарияланған құпия есепте жариялады. Оны 1945 жылы ол қайтадан жариялады Химиялық және инженерлік жаңалықтар, 1949 жылға дейін бірнеше авторлар Seaborg ұсынысына түсініктеме берді және олармен жалпы келіседі. Сол жылы ол актинидтерді презентациялаудың ең жақсы әдісі оларды лантаноидтардың астына және аналогтары ретінде орналастыру арқылы көрінетіндігін атап өтті.[58]
Мұндай аргументтер «жүйені күрт бөлінген блоктарға бөлу қателік» екендігінің дәлелі болып табылады.[59] Үшінші жалпы нұсқа төмендегі екі позицияны көрсетеді иттрий лантаноидтар мен актинидтер алып жатқандықтан. Төртінші нұсқада 3-топ Sc-Y-ден кейін La-Ac тармағына және Lu-Lr тармағына бифуркацияны көрсетеді.[60]
1892 жылы, лютециум табылғанға дейін, Генри Бассетт лантанды скандий мен иттрий бір топқа жатпайды деп санады;[61] 1905 жылы, Альфред Вернер дәл осылай жасады.[62] 1921 жылдан бастап лютеций мен луренцийді қолдау үшін химиялық және физикалық дәлелдер келтірілді[63][64] бірақ авторлардың көпшілігі оларға сенбеген немесе олар туралы білмейтін болып көрінеді.[65][66] Жұмыс істейтін химиктердің көпшілігі ешқандай даудың бар екенін білмейді.[66] 2015 жылдың желтоқсанында IUPAC жоба тек алғашқы екі баламаны ғана қарастыра отырып, мәселе бойынша ұсыныс беру үшін құрылды.[67]
Лантан және актиний
Y-ден төмен La және Ac |
Лантан мен актиний әдетте 3 топтың қалған мүшелері ретінде бейнеленеді.[68][n 4] Бұл макет 1940 жылдары пайда болды, элементтердің негізгі күйіндегі электронды конфигурацияларына және дифференциалданатын электрондар ұғымына сүйенетін периодтық кестелер пайда болды деген болжам жасалды. Негізгі күй конфигурациясы цезий, барий ал лантан - [Xe] 6s1, [Xe] 6с2 және [Xe] 5d16с2. Лантан осылайша 5d дифференциалданатын электронмен шығады және осы негіздер бойынша «6-кезеңдегі d-блоктың бірінші мүшесі ретінде 3-топта» болып саналды.[69] Электрондық конфигурациялардың үстірт жиынтығы 3-топта көрінеді: скандий [Ar] 3d14с2, иттрий [Kr] 4d15с2 және лантан [Xe] 5d16с2. 6-кезеңде, итербиум [Xe] 4f электронды конфигурациясы тағайындалды135к16с2 және лютеий [Xe] 4f145к16с2, «нәтижесінде лютеций үшін 4f дифференциалданатын электрон пайда болады және оны 6-кезеңдегі f-блоктың соңғы мүшесі ретінде мықты орнатады».[69] Кейінірек спектроскопиялық жұмыс итербиумның электронды конфигурациясы шын мәнінде [Xe] 4f екенін анықтады146с2. Бұл итербиум мен лютеций - соңғысы [Xe] 4f дегенді білдіреді145к16с2- екеуінде де 14 f-электрондары болды, нәтижесінде лютеций үшін «f-дифференциалданатын электрон емес, d пайда болды» және оны «Xe] 5d» тең дәрежелі үміткерге «айналдырды.16с2 лантан, 3-топ үшін периодтық жүйе бойынша иттрийден төмен орналасқан.[69] Лантан 5-ші күннен бастап қызмет ету артықшылығына ие1 электрон өзінің құрылымында бірінші рет пайда болса, үшінші рет лутецийде пайда болып, гадолинийде екінші рет пайда болды.[70]
Жердегі газ-фазалық конфигурациялар көбінесе әртүрлі конфигурацияларды көрсететін қосылыстардағы байланыс атомдарынан айырмашылығы тек оқшауланған атомдарды қарастырады (соңғысы химия үшін маңызды).[71] Сонымен қатар, екі түрлі конфигурацияның ең төменгі деңгейлері көбінесе таралумен салыстырғанда өте аз энергиямен бөлінеді Дж- әр конфигурация деңгейлері (мысалы, тербиум, мұнда 285 см−1 [Xe] 4f арасындағы айырмашылық85к16с2 және негізгі күй [Xe] 4f95с2 бұл жайылымның 1% -дан әлдеқайда аз), бұл негізгі күй конфигурациясын химиялық тұрғыдан маңызды емес етеді.[72] Бұл сапалы химиялық әрекетті ұтымды ете алатын вакуумдағы бос газ тәрізді емес, химиялық ортадағы атомдардың басым электронды конфигурациясы.[73]
Итриум астындағы лантанмен формасы торийді емдеуде сәйкессіздік тудырады, оның негізгі күйінде f-электрондары жоқ ([Rn] 6d27с2), актинийге ұқсас [Rn] 6d17с2; ол торийді f-блокқа орналастырады, бірақ актиний емес.[74] Газ-фазалық жердегі конфигурацияларды ғана ескере отырып, торий [Rn] 6d27с2 өздігінен цирконийдің гомологы жақсы [Kr] 4d25с2 лантан ретінде [Xe] 5d16с2 скандий болып табылады [Ar] 3d14с2;[72] торий әрдайым f-блокта орналасады. Осылайша, торий элементтің газ күйіндегі фазалық конфигурациясында f электронын иелену оның f блогына жатуы үшін қажет еместігін көрсетеді.[75] Сонымен қатар, бұл форма 32 бағандық периодтық кестеге дейін кеңейтілген жағдайда d-блокты бөлуді қажет етеді.[75] Сонымен, d-блоктың бөлінбеуі арқылы жүйелілікті немесе симметрияны негізгі талап ретінде қарастыруға негіз жоқ.[76][n 5]
Химиялық мінез-құлық тұрғысынан,[77] және балқу температурасы, электр терістілігі және иондық радиус сияқты қасиеттерге (егер Sc-Y-La таңдалса) 3-топқа түсетін үрдістер,[78][79] скандий, иттрий, лантан және актиний олардың 1-2 аналогтарына ұқсас, бірақ d-блоктың алғашқы тобындағы басқа топтарға сәйкес келмейді. Бұл нұсқада f f-блок элементтерінің ең көп таралған (үш валентті) иондарындағы электрондар олардың f-блогындағы жағдайына сәйкес келеді.[80] Мысалы, f-электрон алғашқы үш f-блок элементтерінің үш валентті иондары үшін есептеледі, Ce 1, Pr 2 және Nd 3.[81]
Жақында скандий, иттрий, лантан және актиний ретінде 3-топқа жүргізілген талдау нәтижесінде мұндай келісім негізге алынды мерзімді заң; басым дифференциалды электрондар; 3-топтың жақын көршілері; көлденең триадалар; изодиагоналдылық; скандийден лантанға және лутетийге монокациялар; табиғаты сирек кездесетін жер; лантаноид немесе f-блоктың жиырылуы; f-блоктың тұтастығы; және ең маңызды электронды орбитальдар.[76]
Лютециум және заң
Y-ден төмен Lu және Lr |
Басқа кестелерде лютециум мен луренций 3 топтың қалған мүшелері болып табылады.[n 6] Скандийді, иттрийді және лютецияны химиялық жолмен бөлудің алғашқы әдістері бұл элементтердің «иттрий тобы» деп аталатын бөліктерінде бірге пайда болғандығына негізделді, ал La мен Ac «церий тобында» бірге пайда болды.[69] Тиісінше, лантаннан гөрі лютецийді 1920-1930 жылдары кейбір химиктер 3-топқа тағайындады. Әр түрлі бөліну топтарының құбылысы радиустың жоғарылауымен негіздіктің жоғарылауынан туындайды және Y-ден төмен емес, Лу-ны көрсету үшін негізгі себеп болмайды. Сонымен, 2 топтың қатарына сілтілі жер металдары, Mg (негізі азырақ) «еритін топқа» жатады, ал Ca, Sr және Ba (негізгілері) «аммоний карбонат тобында» кездеседі. Осыған қарамастан, Mg, Ca, Sr және Ba жүйелі түрде периодтық жүйенің 2-тобында орналасады.[82] Әрі қарай, иттрийдің бөліну тобының мінез-құлқы екі мағыналы болуы мүмкін, ал скандий, иттрий және лантанум лутетийден өзгеше комплекс әрекетін көрсетеді.[83][84]
1950 - 60 жж. Бірнеше физиктер лутетийді лантанмен бірнеше физикалық қасиеттерін салыстыру тұрғысынан жақтады.[69] Осы форманың көрнекті жақтаушылары арасында болды Лев Ландау және Евгений Лифшиц, кім жазды Теориялық физика курсы (1958):[85]
Химия кітаптарында лютециум сирек кездесетін элементтерге орналастырылған. Бірақ бұл дұрыс емес, өйткені 4f қабығы лютецийде толық; сондықтан оны платина тобына енгізу керек [олар La + Lu – Pt деп санайды] ...
— Ландау мен Лифшиц, Теориялық физика курсы, Т. 3: Кванттық механика: релятивистік емес теория (1958)
Лантан f-блогының бірінші мүшесі болып табылатын бұл орналасу туралы кейбір авторлар дау тудырады, өйткені лантанда кез-келген f-электрондары жоқ. Торий сияқты басқа периодтық жүйенің ауытқуларын ескере отырып, бұл дұрыс алаңдаушылық тудырмайды деп айтылды.[86] Құрамында 4f электроны бар лантанның қозған күйлерінің 4f деңгейлерінің байланыс энергиялары лантанның 4f орбитальдарының сутекті емес екенін айқын көрсетеді. Басқаша айтқанда, сутегі барий арқылы 4f орбитальдар ядродан жеткілікті, оларды талдағанда ядро мен қалған электрондарды нүктелік заряд ретінде жуықтауға болады; лантаннан бастап бұл жағдай тоқтатылады, лантан келесі сирек жер деңгейлеріне ұқсас 4f деңгейлерін көрсетеді.[87] Лютеций жетіспейтін бұл төмен бос орбитальдар,[74] кейбір лантандық қосылыстардың қосылуына үлкен үлес қосады, мысалы лантан (III) фтор (LaF3). Бұл үлес аз болғанымен, лантан үшін кез-келген аналогтық LnF-ті ескере отырып, басқа лантанидтерге қарағанда көп болады.3 қосылыс; сонымен қатар LuF-де Lu-F 4f – 2p облигациясы3 осыған ұқсас IrF-тен аз3, бірге иридий жақсы 5d блокқа.[88] Ал үш валентті лантаноидтар Pr3+ Yb арқылы3+ лигандаларға өз позицияларымен дерлік тән тар жолақтарды көрсетіңіз, келесі 5d элементтер (3d және 4d элементтерімен бірге) айтарлықтай өзгеше әрекет етеді; элементтердің екі түрі де электронды тасымалдау жолақтарын көрсетеді, лиганд өрісінің теориясы осы d элементтері үшін маңызды болады.[89] Лантанға 4f қатысу тәртібі 5f торияға ұқсас; церийдегі 4ф-тің урандағы 5ф-қа ұқсас.[72]
| Sc | Ти | V | Cr | Мн | Fe | Co | Ни | Cu | Zn |
|---|---|---|---|---|---|---|---|---|---|
| hp | hp | көшірме | көшірме | ~ көшірме | көшірме | hp | fcc | fcc | ~ hcp |
| Y | Zr | Nb | Мо | Tc | Ru | Rh | Pd | Аг | CD |
| hp | hp | көшірме | көшірме | hp | hp | fcc | fcc | fcc | ~ hcp |
| Лу | Hf | Та | W | Қайта | Os | Ир | Pt | Ау | Hg |
| hp | hp | көшірме | көшірме | hp | hp | fcc | fcc | fcc | ~ hcp |
| Lr | Rf | Db | Сг | Bh | Hs | Mt | Ds | Rg | Cn |
| hp | hp | көшірме | көшірме | hp | hp | fcc | көшірме | көшірме | көшірме |
Ландау мен Лифшицтің позициясы дұрыс түсіндірілмеген және олар 3-топтағы лантан мен лютециумды қолдайды деген болжам жасалды, бұл нұсқа басқа авторлар кейде ұсынған.[76]
Лантанның dhcp кристалды құрылымы стандартты жағдайда ең тұрақты құрылымға ие, ал актиний - fcc; ал скандий, иттрий, лутетий және луренций (соңғы болжам) hcp кристалл құрылымын көрсетеді. Dhcp кристалды құрылымы тек f-блогындағы кейбір сирек металдар мен актинидтермен белгілі және периодтық жүйенің басқа жерлерінде белгісіз.[87] Бұл магниттік емес ауыспалы металдардың кристалдық құрылымдарының олардың валенттілігімен басқаша түрде толығымен тұрақты өзгеруінің ауытқуын құрайды (6д-металдардың соңын қоспағанда, олар өте ауыр элементтер үшін релятивистік әсерлердің әсерінен аномальды болуы керек),[90][91] және лантанға 4ф диапазонының қатысуының белгісі.[90] Керісінше, лантанның қысым-температуралық фазалық диаграммасы даулы емес 4f металдар үшін изоморфты болып табылады. празеодим және неодим.[90] 4f қатысуынсыз празеодимий мен неодимий HCP скандий, иттрий және лутетий сияқты болады деп күтуге болады, бірақ оның орнына лантанум сияқты dhcp болады.[90]
Карл Гшнайнднер 1971 жылғы мақаласында лантаноидтардың балқу температураларын талдай отырып, лантанидті металдарды байланыстыруға 4f, 5d, 6s және 6p электрондарының бәрі қатысқан деген болжам жасады, бұл жерде лютециумнан басқа, 4f электрондары табылмаған. қатысады.[92] Лантанның 4ф диапазонды металл екендігі дәлелденді (FCC лантандағы бір атомда 0,17 электрон бар, бұл стандартты жағдайда метастабильді)[93] ал 4f қабығы лютецийдің металл қасиеттеріне әсер етпейтін сияқты болса, лантанның орнына лютециумды 3-топқа орналастырудың дәлелі ретінде қолданылды.[90] Қатты лантандағы 4f сыйымдылығы оның кейбір қасиеттерін түсіндіруі мүмкін, мысалы оның төмен балқу температурасы (La 920 ° C, Sc 1541 ° C, Y 1526 ° C, Lu 1652 ° C)[92] төмен Дебей температурасы, және барлық қысым кезіндегі ауытқуы жоғары асқын өткізгіштік температура.[90] Шынында да, егер лантанды d-блок элементі ретінде қарастыратын болса, онда ол әртүрлі қысымдағы асқын өткізгіштік ауыспалы температура тенденцияларының ауытқуларын құрайды, егер олардың орнына лютеций қойылса, бәрі жойылады.[87][90] Йорг Виттиг, осы мәселені 1973 жылы қарастыра отырып, лантанға қатысатын бұл 4f диапазонның церий сияқты «лантандық ион ядросының ішкі қабатында сақталған 4f шашыранды резонанстың скринингтік зарядын білдіреді» деген тұжырымға келді: бұл келісімде Gschneidner моделімен. Мұны байқаудағы қиындық виртуалды байланысқан осы 4f күйге ие күшті d резонансына байланысты болады. Мұны LaAl қорытпасы растайды2, бұл дебай температурасы және LuAl-мен салыстырғанда 16% -ға төмен электронды жылу коэффициенттері2 «жағдайларды қосымша 4f тығыздықта» көрсетеді Ферми беті".[90]
Скандий, иттриум және лютеий электронды конфигурациялардың периодтық жүйедегі ғаламдық трендке сәйкес келетін жиынтығын көрсетеді: 5д металдар, содан кейін барлығы жабық 4f қосады14 қабық. Мысалы, иттрийден [Kr] 4d ауысу15с2 люцийге дейін [Xe] 4f145к16с2 циркониймен [Kr] 4d параллель25с2 гафнийге [Xe] 4f145к26с2.[69] Лантаннан гөрі лутецийдің қосылуы 5-ші ауысу серияларын біртектес етеді: атомдық өлшемдер, координациялық сан және метал-оттегі байланыстарының салыстырмалы көптігі лютециумның лантанға қарағанда даулы емес 5д металдар гафнийінің сынап арқылы жүруіне жақын екендігін көрсетеді.[94] (алайда, лутеций иттрийдің астында немесе итербиумнан кейін f-блоктың соңында болғанына қарамастан қолданылады).[76]
Элементтердің өткізгіштік жолақ құрылымдарын қарастырғанда да дәл солай: лютецийдің өтпелі металға ұқсас өткізгіштік жолақ құрылымы бар, ал лантанда болмайды[95] Лантан әлі де өтпелі металдарға тән күйлердің жоғары тығыздығына ие болғандықтан, мұндай типтік емес құрылымның маңызы айқын емес.[96] Лютеций гафний сияқты өтпелі металдарға тән өткізгіштік жолақ құрылымына ие бола тұра, периодтық жүйенің басқа жерлеріндегі өткізгіштік диапазондарының ауытқуларын ескере отырып, бұл ерекше назар аудармайды. Мысалы, ауыр сілтілі металдардың өткізгіштік жолақтары бос d жолақтарының болуына байланысты аномальды мінез-құлық көрсетеді, ал бұл Li және Na үшін болмайды).[97] 3-10 өтпелі металдардың өткізгіштік жолақтары s электрондары мен олардың ішінара толтырылған d қабықшалары арасындағы күрделі өзара әрекеттесулермен сипатталады, ал бұл 11-топтағы монеталар металдары үшін толтырылған d қабығының болуына байланысты емес, сондықтан соңғы металдар көрсетеді жоғары электр және жылу өткізгіштік.[98]
Lawrencium-ға келетін болсақ, оның газ фазалық жердегі атомдық электронды конфигурациясы 2015 жылы [Rn] 5f ретінде расталды147с27p1. Мұндай конфигурация заңның f-немесе d-блогында орналасқанына қарамастан, басқа периодтық кестенің аномалиясын білдіреді, өйткені тек ықтимал қолданылатын р-блок позициясы сақталған нихониум [Rn] 5f болжамды конфигурациясымен146д107с27p1.[99] Дегенмен, конденсацияланған фазада және химиялық ортада луренцийдің күтілетін 6-деңгейге ие болуы күтілуде және қарапайым модельдеу зерттеулері оның өзін лантанид тәрізді ұстайтындығын болжайды,[100] лутетийдің гомологы болу.
Скандий, иттрий және лутетий (және хименциясы белгілі болғанда, лрукренций) көбінесе 1-2 металдардың үш валентті нұсқалары сияқты әрекет етеді, көбінесе топтық тотығу дәрежесімен шектелген А-класты катиондар, олар d-блоктағы немесе f-блоктағы элементтер ғана.[101][бет қажет] 4-топтағы цирконий мен гафний, сондай-ақ 5-топтағы ниобий мен танталдың ауыспалы металдары да осындай мінез көрсетеді,[101][бет қажет] актинидті торий сияқты.[102] (Ауыр топтың 4 элементі мен торий төрт валентті, 5 ауыр топтың элементтері бес валентті.)[102][103] 3-топ элементтерінің физикалық қасиеттеріне d электронының қатысуы әсер етеді, олар металдар ішінде 13-топтағы ұқсас металдардағы p электрондарына қарағанда локализацияланған байланыстар түзеді;[104] 4-топ пен 14-топты салыстыра отырып, дәл осындай жағдай кездеседі.[105] Балқу температурасы, электронды терімділік және иондық радиус сияқты қасиеттер бойынша 3 топқа (егер Sc-Y-Lu таңдалса) төмен түсетін үрдістер, сол блоктағы 4-8 аналогтарының арасында кездесетінге ұқсас, Вильям Б. Дженсен 1982 жылы жиі келтірілген мақаласында ол осы орналастыру туралы пікір айтқан.[69] Бұл нұсқада f f-блок атомдарының газ тәрізді формасындағы электрондар, әдетте, f-блоктағы өз орындарына сәйкес келеді. Мысалы, f-электронның алғашқы бес блок-элементі үшін La 0, Ce 1, Pr 3, Nd 4 және Pm 5 есептелінеді.[69]
Лантаноидтар мен актинидтер
Y-ден төмен белгілер |
Бірнеше автор барлық отыз лантаноидтар мен актинидтерді иттрийден төмен орналасқан екі позицияға орналастырады (әдетте сілтеме белгілері арқылы). Бұл нұсқа 2005 ж. Қызыл кітап 2005 жылдан бастап IUPAC келіскен нұсқасы болуы керек (бірқатар кейінгі нұсқалары бар, ал соңғы жаңарту 2018 жылдың 1 желтоқсанынан бастап),[106][n 7] 15 лантанидті элементтердің (Ла-Лу) химиясындағы ұқсастықтарды, мүмкін екіұштылық есебінен, элементтердің екі топқа итрийден төмен 3 позицияны иеленетіндігі және ені 15 бағаналы екендігіне баса назар аударады f блок (кез келген қатарда тек 14 элемент болуы мүмкін f блок).[n 8] Алайда, бұл ұқсастық химикаттарында анағұрлым кең әртүрлілікті көрсететін 15 актинидті элементтерге (Ac-Lr) таралмайды.[72] Бұл форма сонымен қатар f-блокты d-блоктың 3-тобының деградацияланған тармағына дейін азайтады; ол 1920 жылдары лантаноидтар өздерінің f электрондары негізгі электрондар деп ойлаған кезде пайда болды, ол қазір жалған болып саналады. Бұл актинидтер үшін де жалған, олардың көпшілігі тұрақты тотығу дәрежесін +3 жоғары көрсетеді.[108]
La-Ac және Lu-Lr
Бұл нұсқада 3-топ Sc-Y-ден кейін La-Ac тармағына және Lu-Lr тармағына бифуркатталады. Бұл келісім химиялық және физикалық деректерге негізделген Sc-Y-La-Ac немесе Sc-Y-Lu-Lr пайдасына дәлелдер нәтижесіз деген гипотезамен сәйкес келеді.[109] Белгіленгендей, Sc-Y-La-Ac төмендеу үрдістері 1−2 топтарындағы тенденцияларға сәйкес келеді[110] ал Sc-Y-Lu-Lr төмендеу тенденциялары 4−10 топтарындағы тенденцияларға сәйкес келеді.[69]
3 топтың бифуркациясы - Менделеевтің сегіз баған формасына лақтыру, мұнда негізгі топтардың жетеуінде екі кіші топ бар. Осы уақыттан бастап бифуркацияланған 3 тобы бар кестелер мезгіл-мезгіл ұсынылып келеді.[n 9]
Пайда болу
Скандий, иттрий, лантаний және лютеий жер қыртысының басқа лантаноидтарымен (прометийден басқа) бірге жүруге бейім, оларды көбінесе олардың кендерінен алу қиынырақ. The жер қыртысының элементтерінің көптігі 3 топ үшін өте төмен - топтағы барлық элементтер сирек кездеседі, олардың ең көп мөлшері - иттриум, олардың саны шамамен 30миллионға бөлшектер (ppm); скандийдің көптігі 16 промилле, ал лютеций шамамен 0,5 промилл. Лантанның көптігі шамамен 35 адам / мин құрайды. Салыстыру үшін мыс көптігі - 50 промилле, хромдікі - 160 промилл, ал молибден - 1,5 промилле.[111]
Скандий сирек таралады және көп мөлшерде кездеседі минералдар.[112] Скандинавиядан сирек кездесетін минералдар[113] және Мадагаскар[114] сияқты гадолинит, эвсенит, және тортвейтит осы элементтің белгілі шоғырланған жалғыз көзі болып табылады, соңғысында құрамында 45% дейін скандий бар скандий (III) оксиді.[113] Итрийдің пайда болу орындарында бірдей тенденциясы бар; кезінде жиналған ай жыныстарының үлгілерінде кездеседі Американдық Аполлон жобасы салыстырмалы түрде жоғары мазмұнда.[115]

Лутетийдің негізгі коммерциялық пайдалы кендері сирек кездесетін жер болып табылады фосфат минерал моназит, (Ce, La, және т.б.) PO4, оның құрамында 0,003% элемент бар. Негізгі тау-кен аймақтары Қытай, АҚШ, Бразилия, Үндістан, Шри-Ланка және Австралия. Таза лютеий металл - бұл сирек кездесетін металдардың бірі, бағасы шамамен 10000 АҚШ доллары / кг, немесе шамамен төрттен бірі алтын. Лантан өте сирек кездеседі, сирек кездесетін екінші жер болғандықтан, моназиттен басқа экономикалық жағынан да оны алуға болады. баст.[116][117]
Өндіріс
3 топтағы ең қол жетімді элемент - иттрий, оның жылдық өндірісі 8900 құрайдытонна Итрий көбінесе төмендегідей өндіріледі оксид, бір ел, Қытай (99%).[118] Лутеций мен скандий көбінесе оксидтер түрінде алынады, ал олардың жылдық өндірісі 2001 жылға қарай шамамен 10 және 2 тоннаны құрады.[119]
3-топ элементтері басқа элементтердің экстракциясынан алынған қосымша өнім ретінде ғана өндіріледі.[120] The metallic elements are extremely rare; the production of metallic yttrium is about a few tonnes, and that of scandium is in the order of 10 kg per year;[120][121] production of lutetium is not calculated, but it is certainly small. The elements, after purification from other rare-earth metals, are isolated as oxides; the oxides are converted to fluorides during reactions with hydrofluoric acid.[122] The resulting fluorides are төмендетілді бірге сілтілі жер металдары or alloys of the metals; металл кальций is used most frequently.[122] Мысалға:
- Sc2O3 + 3 HF → 2 ScF3 + 3 H2O
- 2 ScF3 + 3 Ca → 3 CaF2 + 2 Sc
Биологиялық химия
Group 3 elements are generally hard metals with low aqueous solubility, and have low availability to the biosphere. No group 3 element has any documented biological role in living organisms. The radioactivity of the actinides generally makes them highly toxic to living cells, causing радиациялық улану.
Scandium has no biological role, but it is found in living organisms. Once reached a human, scandium concentrates in the liver and is a threat to it; some its compounds are possibly канцерогенді, even through in general scandium is not toxic.[123] Scandium is known to have reached the food chain, but in trace amounts only; a typical human takes in less than 0.1 micrograms per day.[123] Once released into the environment, scandium gradually accumulates in soils, which leads to increased concentrations in soil particles, animals and humans. Scandium is mostly dangerous in the working environment, due to the fact that damps and gases can be inhaled with air. This can cause lung embolisms, especially during long-term exposure. The element is known to damage cell membranes of water animals, causing several negative influences on reproduction and on the functions of the nervous system.[123]
Итрийдің белгілі биологиялық рөлі жоқ, дегенмен ол организмдердің барлығында болмаса да, көпшілігінде кездеседі және бауырда, бүйректе, көкбауырда, өкпеде және сүйектерде шоғырлануға бейім.[124] There is normally as little as 0.5 milligrams found within the entire human body; адам емшек сүті 4 промилл бар.[125] Итриумды жеуге жарайтын өсімдіктерде 20 промилле мен 100 ррм (жаңа салмақ) арасындағы концентрацияда кездестіруге болады. орамжапырақ ең үлкен сомаға ие.[125] With up to 700 ppm, the seeds of woody plants have the highest known concentrations.[125]
Lutetium has no biological role as well, but it is found even in the highest known organism, the адамдар, concentrating in bones, and to a lesser extent in the liver and kidneys.[126] Lutetium salts are known to cause metabolism and they occur together with other lanthanide salts in nature; the element is the least abundant in the human body of all lanthanides.[126] Human diets have not been monitored for lutetium content, so it is not known how much the average human takes in, but estimations show the amount is only about several micrograms per year, all coming from tiny amounts taken by plants. Soluble lutetium salts are mildly toxic, but insoluble ones are not.[126] Lanthanum is not essential for humans and has a low to moderate level of toxicity. However, it is essential for the метанотрофты бактерия Methylacidiphilum fumariolicum SolV, although the general similarity of the rare earths means that it may be substituted by some of the other early lanthanides with no ill effects.[127]
The high radioactivity of lawrencium would make it highly toxic to living cells, causing radiation poisoning. The same is true for actinium.
Ескертулер
- ^ Итербит жақын жерде табылған ауылдың атымен аталды, сонымен бірге оның минерал екенін көрсететін аяқталған жер.
- ^ Жерге -а, ал жаңа элементтерге -ium шегі беріледі.
- ^ Unpenttrium, according to calculations, should have an electronic configuration of [Og]8s25г186f117д28p1/22.[37]
- ^ For examples of this table see Аткинс т.б. (2006). Шрайвер және Аткинс бейорганикалық химия (4-ші басылым). Oxford: Oxford University Press • Myers et al. (2004). Holt Chemistry. Orlando: Holt, Rinehart & Winston • Chang R. (2000). Essential Chemistry (2-ші басылым). Бостон: МакГрав-Хилл
- ^ Vernon considers increasing regularity in the shape of the periodic table to increase the number of irregularities amongst various other properties and relationships across the table. See: Vernon R.E. 2020. The location and composition of Group 3 of the periodic table. Foundations of Chemistry.
- ^ For examples of the group 3 = Sc-Y-Lu-Lr table see Rayner-Canham G. & Overton T. (2013). Descriptive Inorganic Chemistry (6-шы басылым). New York: W. H. Freeman and Company • Brown et al. (2009). Химия: Орталық ғылым (11-ші басылым). Upper Saddle River, New Jersey: Pearson Education • Moore et al. (1978). Химия. Tokyo: McGraw-Hill Kogakusha
- ^ Notwithstanding, an IUPAC member subsequently wrote that, "IUPAC has not approved any specific form of the periodic table, and an IUPAC-approved form does not exist, though even members of IUPAC themselves have published diagrams titled “IUPAC Periodic Table of the Elements". However, the only specific recommendation IUPAC has made concerning the periodic table covers the Group numbering of 1–18."[107]
- ^ For examples of the group 3 = Ln and An table see Housecroft C. E. & Sharpe A. G. (2008). Бейорганикалық химия (3-ші басылым). Harlow: Pearson Education • Halliday et al. (2005). Физика негіздері (7-ші басылым). Hoboken, New Jersey: John Wiley & Sons • Nebergall et al. (1980). General Chemistry (6-шы басылым). Lexington: D. C. Heath and Company
- ^
- 1922 Bohr's system, with bifurcations at Na, Mg, and Y
- 1939 Foster LS, [https://www.meta-synthesis.com/webbook/35_pt/pt_database.php?PT_id=1056 "Why not modernise textbooks also? I. The periodic table", Химиялық білім журналы, т. 16, жоқ. 9. In group 3 the box under Y is “La {58–70}* Lu”, where * = the rare earths.
- 1947 Stedman's planar arrangement оның conic system
- 1952 Coryell, shows a step pyramid style table, with solid and dashed tie lines to show primary and secondary relationships. Just two elements are shown by him as having two solid tie lines: yttrium, to La-Ac and to Lu-Ac; and silicon, to Ti-Zr-Hf and to Ge-Sn-Pb.
- 1964 Sanderson RT, "A rational periodic table", Journal of Chemical Education, т. 41, жоқ. 4, pp. 187–189
- 1974 Mazurs EG, Graphic representations of the periodic system during one hundred years, The University of Alabama Press, Alabama, p. 77
- 2020 Vernon RE, "Organising the metals and nonmetals", Foundations of Chemistry, open access, see Electronic supplementary material
Әдебиеттер тізімі
- ^ ван дер Крогт, Петр. "39 Yttrium – Elementymology & Elements Multidict". Elements.vanderkrogt.net. Алынған 2008-08-06.
- ^ Эмсли 2001 ж, б. 496
- ^ Гадолин, Йохан (1794). «Stenart iftån Ytterby Stenbrott i Roslagen туралы». Конгл. Vetenskaps Academiens Nya Handlingar (швед тілінде). 15: 137–155.
- ^ Гринвуд, Н. Эрншоу, А. (1997). Элементтер химиясы (2-ші басылым). Оксфорд: Баттеруорт-Хейнеманн. б. 944. ISBN 0-7506-3365-4.
- ^ Коплен, Тайлер Б .; Peiser, H. S. (1998). «1882-1997 жылдар аралығында ұсынылған атомдық-салмақтық құндылықтардың тарихы: қазіргі мәндерден бұрынғы мәндердің болжамды белгісіздіктерімен айырмашылықтарын салыстыру (техникалық есеп)». Таза Appl. Хим. IUPAC's Inorganic Chemistry Division Commission on Atomic Weights and Isotopic Abundances. 70 (1): 237–257. дои:10.1351 / pac199870010237. S2CID 96729044.
- ^ Хейзерман, Дэвид Л. (1992). "Element 39: Yttrium". Химиялық элементтер мен олардың қосылыстарын зерттеу. Нью-Йорк: TAB Books. 150–152 бет. ISBN 0-8306-3018-X.
- ^ Вёлер, Фридрих (1828). "Über das Beryllium und Yttrium". Аннален дер Физик (неміс тілінде). 89 (8): 577–582. Бибкод:1828AnP .... 89..577W. дои:10.1002 / және.18280890805.
- ^ Ball, Philip (2002). The Ingredients: A Guided Tour of the Elements. Оксфорд университетінің баспасы. 100-102 бет. ISBN 0-19-284100-9.
- ^ Nilson, Lars Fredrik (1879). "Sur l'ytterbine, terre nouvelle de M. Marignac". Comptes Rendus (француз тілінде). 88: 642–647.
- ^ Nilson, Lars Fredrik (1879). "Ueber Scandium, ein neues Erdmetall". Berichte der deutschen chemischen Gesellschaft (неміс тілінде). 12 (1): 554–557. дои:10.1002/cber.187901201157.
- ^ Cleve, Per Teodor (1879). "Sur le scandium". Comptes Rendus (француз тілінде). 89: 419–422.
- ^ Fischer, Werner; Brünger, Karl; Grieneisen, Hans (1937). "Über das metallische Scandium". Zeitschrift für anorganische und allgemeine Chemie (неміс тілінде). 231 (1–2): 54–62. дои:10.1002/zaac.19372310107.
- ^ "The Discovery and Naming of the Rare Earths". Elements.vanderkrogt.net. Алынған 23 маусым 2016.
- ^ а б Гринвуд және Эрншоу, б. 1424
- ^ Апта, Мэри Эльвира (1932). «Элементтердің ашылуы: XI. Калий мен натрий көмегімен оқшауланған кейбір элементтер: цирконий, титан, церий және торий». The Journal of Chemical Education. 9 (7): 1231–1243. Бибкод:1932JChEd ... 9.1231W. дои:10.1021 / ed009p1231.
- ^ Қараңыз:
- (Берцелиус) (1839) «Nouveau métal» (Жаңа металл), Comptes rendus, 8 : 356–357. Б. 356: "L'oxide de cérium, extrait de la cérite par la procédé ordinaire, contient à peu près les deux cinquièmes de son poids de l'oxide du nouveau métal qui ne change que peu les propriétés du cérium, et qui s'y tient pour ainsi dire caché. Cette raison a engagé M. Mosander à donner au nouveau métal le nom de Лантан." (The oxide of cerium, extracted from cerite by the usual procedure, contains almost two fifths of its weight in the oxide of the new metal, which differs only slightly from the properties of cerium, and which is held in it so to speak "hidden". This reason motivated Mr. Mosander to give to the new metal the name Лантан.)
- (Берцелиус) (1839) «Латани - жаңа металл» Философиялық журнал, жаңа серия, 14 : 390–391.
- ^ а б Патнаик, Прадёт (2003). Бейорганикалық химиялық қосылыстар туралы анықтама. McGraw-Hill. pp. 444–446. ISBN 0-07-049439-8. Алынған 2009-06-06.
- ^ Urbain, M. G. (1908). «Un nouvel élément, le lutécium, résultant du dédoublement de l'ytterbium de Marignac». Comptes rendus (француз тілінде). 145: 759–762.
- ^ «Сирек жер элементтерін Чарльз Джеймс бөлуі». Ұлттық тарихи химиялық бағдарлар. Американдық химиялық қоғам. Алынған 2014-02-21.
- ^ von Welsbach; Carl Auer (1908). «Die Zerlegung des Ytterbiums in seine Elemente». Monatshefte für Chemie (неміс тілінде). 29 (2): 181–225. дои:10.1007 / BF01558944. S2CID 197766399.
- ^ Урбаин, Г. (1909). «Lutetium und Neoytterbium oder Cassiopeium und Aldebaranium - Erwiderung auf den Artikel des Herrn Auer v. Welsbach». Monatshefte für Chemie (неміс тілінде). 31 (10): I. дои:10.1007 / BF01530262. S2CID 101825980.
- ^ Clarke, F. W.; Ostwald, W.; Торп, Т .; Урбаин, Г. (1909). "Bericht des Internationalen Atomgewichts-Ausschusses für 1909". Berichte der Deutschen Chemischen Gesellschaft (неміс тілінде). 42 (1): 11–17. дои:10.1002/cber.19090420104.
- ^ ван дер Крогт, Петр. "70. Ytterbium – Elementymology & Elements Multidict". Elements.vanderkrogt.net. Алынған 4 шілде 2011.
- ^ ван дер Крогт, Петр. "71. Lutetium – Elementymology & Elements Multidict". Elements.vanderkrogt.net. Алынған 4 шілде 2011.
- ^ Эмсли, Джон (2001). Табиғаттың құрылыс материалдары: элементтерге арналған A-Z нұсқаулығы. АҚШ: Оксфорд университетінің баспасы. 240–242 бет. ISBN 0-19-850341-5.
- ^ Дебьер, Андре-Луи (1899). «Sur un nouvelle matière радио-белсенді». Comptes rendus (француз тілінде). 129: 593–595.
- ^ Дебьер, Андре-Луис (1900–1901). «Sur un nouvelle matière radio-actif - l'actinium». Comptes rendus (француз тілінде). 130: 906–908.
- ^ Жизель, Фридрих Оскар (1902). «Ueber Radium und radioactive Stoffe». Berichte der Deutschen Chemischen Gesellschaft (неміс тілінде). 35 (3): 3608–3611. дои:10.1002 / cber.190203503187.
- ^ Гизель, Фридрих Оскар (1904). «Ueber den Emanationskörper (Emanium)». Berichte der Deutschen Chemischen Gesellschaft (неміс тілінде). 37 (2): 1696–1699. дои:10.1002 / cber.19040370280.
- ^ Дебьер, Андре-Луи (1904). «Sur l'actinium». Comptes rendus (француз тілінде). 139: 538–540.
- ^ Гизель, Фридрих Оскар (1904). «Ueber Emanium». Berichte der Deutschen Chemischen Gesellschaft (неміс тілінде). 37 (2): 1696–1699. дои:10.1002 / cber.19040370280.
- ^ Жизель, Фридрих Оскар (1905). «Ueber Emanium». Berichte der Deutschen Chemischen Gesellschaft (неміс тілінде). 38 (1): 775–778. дои:10.1002 / cber.190503801130.
- ^ а б Джорсо, Альберт; Сиккеланд, Т .; Larsh, A. E.; Latimer, R. M. (1961). "New Element, Lawrencium, Atomic Number 103" (PDF). Физ. Летт. 6 (9): 473. Бибкод:1961PhRvL...6..473G. дои:10.1103/PhysRevLett.6.473.
- ^ Flerov, G. N. (1967). "On the nuclear properties of the isotopes 256103 and 257103". Ядро. Физ. A. 106 (2): 476. Бибкод:1967NuPhA.106..476F. дои:10.1016/0375-9474(67)90892-5.
- ^ Donets, E. D.; Shchegolev, V. A.; Ermakov, V. A. (1965). "Synthesis of the isotope of element 103 (lawrencium) with mass number 256". Атомная Энергия (орыс тілінде). 19 (2): 109.
- Аударылған Donets, E. D.; Shchegolev, V. A.; Ermakov, V. A. (1965). "Synthesis of the isotope of element 103 (lawrencium) with mass number 256". Кеңестік атом энергиясы. 19 (2): 109. дои:10.1007/BF01126414. S2CID 97218361.
- ^ Гринвуд, Норман Н. (1997). "Recent developments concerning the discovery of elements 101–111". Таза Appl. Хим. 69 (1): 179–184. дои:10.1351/pac199769010179.
- ^ а б c Хоффман, Дарлиан С .; Ли, Диана М .; Першина, Валерия (2006). «Трансактинидтер және болашақ элементтер». Морсада; Эдельштейн, Норман М .; Фужер, Жан (ред.) Актинид және трансактинид элементтерінің химиясы (3-ші басылым). Дордрехт, Нидерланды: Springer Science + Business Media. ISBN 1-4020-3555-1.
- ^ Pyykkö, Pekka (2011). "A suggested periodic table up to Z ≤ 172, based on Dirac–Fock calculations on atoms and ions". Физикалық химия Химиялық физика. 13 (1): 161–8. Бибкод:2011PCCP...13..161P. дои:10.1039/c0cp01575j. PMID 20967377.
- ^ Nefedov, V.I.; Trzhaskovskaya, M.B.; Yarzhemskii, V.G. (2006). "Electronic Configurations and the Periodic Table for Superheavy Elements" (PDF). Doklady физикалық химия. 408 (2): 149–151. дои:10.1134/S0012501606060029. ISSN 0012-5016. S2CID 95738861.
- ^ Hofmann, Sigurd (2002). On Beyond Uranium. Тейлор және Фрэнсис. б.105. ISBN 978-0-415-28496-7.
- ^ Roberto, J. B. (31 March 2015). "Actinide Targets for Super-Heavy Element Research" (PDF). cyclotron.tamu.edu. Техас университеті. Алынған 28 сәуір 2017.
- ^ ван дер Крогт, Петр. "Elementymology & Elements Multidict". Elements.vanderkrogt.net. Алынған 4 шілде 2011.
- ^ Элиав, Е .; Калдор, У .; Ishikawa, Y. (1995). "Transition energies of ytterbium, lutetium, and lawrencium by the relativistic coupled-cluster method". Физ. Аян. 52 (1): 291–296. Бибкод:1995PhRvA..52..291E. дои:10.1103/PhysRevA.52.291. PMID 9912247.
- ^ Zou, Yu; Froese, Fischer C. (2002). "Resonance Transition Energies and Oscillator Strengths in Lutetium and Lawrencium". Физ. Летт. 88 (18): 183001. Бибкод:2002PhRvL..88b3001M. дои:10.1103/PhysRevLett.88.023001. PMID 12005680.
- ^ Корбетт, Дж. Д. (1981). "Extended metal-metal bonding in halides of the early transition metals". Acc. Хим. Res. 14 (8): 239–246. дои:10.1021/ar00068a003.
- ^ Николай Б., Михеев; Ауэрман, Л.Н .; Румер, Игорь А .; Каменская, Алла Н .; Қазақевич, М.З. (1992). «2+ лантаноидтар мен актинидтердің тотығу дәрежесінің аномальды тұрақтануы». Ресейлік химиялық шолулар. 61 (10): 990–998. Бибкод:1992RuCRv..61..990M. дои:10.1070 / RC1992v061n10ABEH001011.
- ^ Канг, Уитюнг; Bernstein, E. R. (2005). «Импульсті лазерлік булануды қолдана отырып, иттрий оксиді кластерін қалыптастыру». Өгіз. Корей химиясы. Soc. 26 (2): 345–348. дои:10.5012 / bkcs.2005.26.2.345.
- ^ Cotton, S. A. (1994). "Scandium, Yttrium and the Lanthanides: Inorganic and Coordination Chemistry". Encyclopedia of Inorganic Chemistry. Джон Вили және ұлдары. ISBN 0-471-93620-0.
- ^ а б Dean, John A. (1999). Lange's handbook of chemistry (Он бесінші басылым). McGraw-Hill, Inc. pp. 589–592. ISBN 0-07-016190-9.
- ^ а б Barbalace, Kenneth. "Periodic Table of Elements Sorted by Melting Point". Environmental Chemistry.com. Алынған 2011-05-18.
- ^ а б Barbalace, Kenneth. "Periodic Table of Elements Sorted by Boiling Point". Environmental Chemistry.com. Алынған 2011-05-18.
- ^ Fournier, Jean-Marc (1976). "Bonding and the electronic structure of the actinide metals". Қатты дене физикасы және химиясы журналы. 37 (2): 235–244. Бибкод:1976JPCS...37..235F. дои:10.1016/0022-3697(76)90167-0.
- ^ Penneman, R. A.; Mann, J. B. (1976). «'Calculation chemistry' of the superheavy elements; comparison with elements of the 7th period". Proceedings of the Moscow Symposium on the Chemistry of Transuranium Elements: 257–263. дои:10.1016/B978-0-08-020638-7.50053-1.
- ^ Лиде, Д.Р., ред. (2003). CRC химия және физика бойынша анықтамалық (84-ші басылым). Boca Raton, FL: CRC Press.
- ^ Barbalace, Kenneth. "Scandium". Химиялық кітап. Алынған 2011-05-18.
- ^ Barbalace, Kenneth. «Итрий». Химиялық кітап. Алынған 2011-05-18.
- ^ Thyssen, P.; Binnemans, K. (2011). Gschneidner Jr., K. A.; Bünzli, J-C.G; Vecharsky, Bünzli (eds.). Accommodation of the Rare Earths in the Periodic Table: A Historical Analysis. Handbook on the Physics and Chemistry of Rare Earths. 41. Амстердам: Эльзевье. 1-94 бет. дои:10.1016/B978-0-444-53590-0.00001-7. ISBN 978-0-444-53590-0.
- ^ Thyssen P. and Binnemans K. (2011). "Accommodation of the Rare Earths in the Periodic Table: A Historical Analysis". In K. A. Gschneider Jr. (ed). Handbook on the Physics and Chemistry of the Rare Earths. 41. Amsterdam: Elsevier, pp. 1–94; Seaborg G. T. (1994). Origin of the Actinide Concept'. In K. A. Gschneider Jr. (ed). Handbook on the Physics and Chemistry of the Rare Earths. 18. Amsterdam: Elsevier, pp. 1–27.
- ^ Stewart, P. J. (2008). "The Flyleaf Table: An Alternative". Химиялық білім журналы. 85 (11): 1490. Бибкод:2008JChEd..85.1490S. дои:10.1021/ed085p1490.
- ^ Сілтеме қатесі: аталған сілтеме
McGraw-Hillшақырылған, бірақ ешқашан анықталмаған (қараңыз анықтама беті). - ^ Henry Bassett, “A Tabular Expression of the Periodic Relations of the Elements”. Chemical News 65 (1892): 3-4, 19
- ^ Alfred Werner, “Beitrag zum Ausbau des periodischen Systems”. Berichte der deutschen chemischen Gesellschaft 38 (1905), 916. дои:10.1002/cber.190503801163
- ^ Thyssen, P.; Binnemanns, K. (2011). "1: Accommodation of the rare earths in the periodic table: A historical analysis". In Gschneidner Jr., K. A.; Büzli, J-C. Дж .; Pecharsky, V. K. (eds.). Handbook on the Physics and Chemistry of Rare Earths. 41. Амстердам: Эльзевье. 80-81 бет. ISBN 978-0-444-53590-0.
- ^ Keeler, J.; Wothers, P. (2014). Chemical Structure and Reactivity: An Integrated Approach. Оксфорд: Оксфорд университеті. б. 259. ISBN 978-0-19-960413-5.
- ^ Скерри, Э. (2012). "Mendeleev's Periodic Table Is Finally Completed and What To Do about Group 3?". Халықаралық химия. 34 (4). дои:10.1515/ci.2012.34.4.28. Мұрағатталды түпнұсқадан 2017 жылғы 5 шілдеде.
- ^ а б Castelvecchi, D. (8 April 2015). "Exotic atom struggles to find its place in the periodic table". Табиғат. дои:10.1038/nature.2015.17275. S2CID 123548806. Мұрағатталды түпнұсқадан 2015 жылғы 5 қазанда. Алынған 20 қыркүйек 2015.
- ^ "The constitution of group 3 of the periodic table". IUPAC. 2015 ж. Мұрағатталды from the original on 5 July 2016. Алынған 30 шілде 2016.
- ^ Emsley, J. (2011). Табиғаттың құрылыс блоктары (жаңа ред.). Оксфорд: Оксфорд университеті. б. 651. ISBN 978-0-19-960563-7.
- ^ а б c г. e f ж сағ мен William B. Jensen (1982). "The Positions of Lanthanum (Actinium) and Lutetium (Lawrencium) in the Periodic Table". Дж.Хем. Білім беру. 59 (8): 634–636. Бибкод:1982JChEd..59..634J. дои:10.1021/ed059p634.
- ^ Trifonov, D. N. (1970). Rare-earth elements and their position in the periodic system (translated from Russian). New Delhi: Indian National Scientific Documentation Centre. 201–202 бет.
- ^ Scerri, Eric (2016). "The Changing Views of a Philosopher of Chemistry on the Question of Reduction". In Scerri, Eric; Fisher, Grant (eds.). Essays in the Philosophy of Chemistry. Оксфорд университетінің баспасы.
- ^ а б c г. Йоргенсен, Кристиан К. (1988). «Сирек кездесетін элементтердің химиялық түсінікке және классификацияға әсері». Handbook on the Physics and Chemistry of Rare Earths. 11. 197–292 беттер. дои:10.1016 / S0168-1273 (88) 11007-6. ISBN 9780444870803.
- ^ Schwarz, W. H. Eugen (2010). "The Full Story of the Electron Configurations of the Transition Elements". Химиялық білім журналы. 87 (4): 444–8. дои:10.1021/ed8001286.
- ^ а б Jensen, William B. (2009). "Misapplying the Periodic Law" (PDF). Химиялық білім журналы. 86 (10): 1186. Бибкод:2009JChEd..86.1186J. дои:10.1021/ed086p1186. Алынған 16 мамыр 2020.
- ^ а б Scerri, Eric (2009). "Which Elements Belong in Group 3?". Химиялық білім журналы. 86 (10): 1188. Бибкод:2009JChEd..86.1188S. дои:10.1021/ed086p1188.
- ^ а б c г. Vernon, R. E. (2020). "The location and composition of Group 3 of the periodic table". Химияның негіздері. дои:10.1007/s10698-020-09384-2.
- ^ Гринвуд, Н. Harrington, T. J. (1973). The chemistry of the transition elements. Оксфорд: Clarendon Press. б.50. ISBN 978-0-19-855435-6.
- ^ Aylward, G.; Findlay, T. (2008). SI химиялық деректері (6-шы басылым). Milton, Queensland: John Wiley & Sons. ISBN 978-0-470-81638-7.
- ^ Wiberg, N. (2001). Бейорганикалық химия. Сан-Диего: академиялық баспасөз. б. 119. ISBN 978-0-12-352651-9.
- ^ Wulfsberg, G. (2006). "Periodic table: Trends in the properties of the elements". Encyclopedia of Inorganic Chemistry. Нью-Йорк: Джон Вили және ұлдары. б. 3. ISBN 978-0-470-86210-0.
- ^ Cotton, S. (2007). Лантанид және актинид химиясы. Чичестер: Джон Вили және ұлдары. б. 150. ISBN 978-0-470-01006-8.
- ^ Moeller et al. (1989). Chemistry with Inorganic Qualitative Analysis (3-ші басылым). SanDiego: Harcourt Brace Jovanovich, pp. 955–956, 958.
- ^ R. C. Vickery (1960). The Chemistry of Yttrium and Scandium. Pergamon Press. б. 37.
- ^ R. C. Vickery (1960). Кешенді бейорганикалық химия. 3. Pergamon Press. pp. 329–354 (344).
- ^ L. D. Landau, E. M. Lifshitz (1958). Кванттық механика: релятивистік емес теория. Том. 3 (1-ші басылым). Pergamon Press. pp. 256–7.
- ^ Scerri, E. (15 September 2015). "Five ideas in chemical education that must die – Group three". Education in Chemistry. Корольдік химия қоғамы. Мұрағатталды түпнұсқадан 23 желтоқсан 2015 ж. Алынған 19 қыркүйек 2015.
It is high time that the idea of group 3 consisting of Sc, Y, La and Ac is abandoned
- ^ а б c Hamilton, David C. (1965). "Position of Lanthanum in the Periodic Table". Американдық физика журналы. 33 (8): 637–640. дои:10.1119/1.1972042.
- ^ Сю, Вэй; Ji, Wen-Xin; Qiu, Yi-Xiang; Schwarz, W. H. Eugen; Wang, Shu-Guang (2013). "On structure and bonding of lanthanoid trifluorides LnF3 (Ln = La to Lu)". Физикалық химия Химиялық физика. 2013 (15): 7839–47. Бибкод:2013PCCP...15.7839X. дои:10.1039/C3CP50717C. PMID 23598823.
- ^ Сілтеме қатесі: аталған сілтеме
Jorgensen2шақырылған, бірақ ешқашан анықталмаған (қараңыз анықтама беті). - ^ а б c г. e f ж сағ Wittig, Jörg (1973). "The pressure variable in solid state physics: What about 4f-band superconductors?". In H. J. Queisser (ed.). Festkörper Probleme: Plenary Lectures of the Divisions Semiconductor Physics, Surface Physics, Low Temperature Physics, High Polymers, Thermodynamics and Statistical Mechanics, of the German Physical Society, Münster, March 19–24, 1973. Қатты дене физикасының жетістіктері. 13. Берлин, Гайдельберг: Шпрингер. б. 375–396. дои:10.1007/BFb0108579. ISBN 978-3-528-08019-8.
- ^ Östlin, A. (2013). "Transition metals" (PDF). Electronic Structure Studies and Method Development for Complex Materials (Лицензиялау). б. 13. Алынған 17 мамыр 2020.
- ^ а б Gschneidner Jr., K. A. (December 1971). "On the nature of 4ƒ bonding in the lanthanide elements and their compounds". Аз таралған металдар журналы. 25 (4): 405–422. дои:10.1016/0022-5088(71)90184-6.
- ^ Glotzel, D. (1978). "Ground-state properties of f band metals: lanthanum, cerium and thorium". Физика журналы F: Металл физикасы. 8 (7): L163–L168. Бибкод:1978JPhF....8L.163G. дои:10.1088/0305-4608/8/7/004.
- ^ Alvarez, Santiago (11 February 2020). "The transition from 4f to 5d elements from the structural point of view". CrystEngComm. 2020 (Advance Article). дои:10.1039/D0CE00029A.
- ^ Merz, H.; Ulmer, K. (1967). "Position of Lanthanum and Lutetium in the Periodic Table". Физика хаттары. 26 (1): 6–7. Бибкод:1967PhLA...26....6M. дои:10.1016/0375-9601(67)90527-0.
- ^ Goncharova, VA; Il'ina, GG (1084). "Anomalies in the elastic properties of polycrystalline lanthanum at phase transitions under pressure". Кеңестік физика JETP. 59 (5): 995–998.
- ^ Smith, NV; Wertheim, GK; Andrews, AB; Chen, C-T (1993). "Inelastic electron mean free paths in the alkali metals". Беттік ғылыми хаттар. 282 (1–2): L359–L363. дои:10.1016/0039-6028(93)90604-I.
- ^ Russell, AM; Lee, KL (2005). Structure-property relations in nonferrous metals. New York: Wiley-Interscience. б. 302.
- ^ Jensen, W. B. (2015). "Some Comments on the Position of Lawrencium in the Periodic Table" (PDF). Архивтелген түпнұсқа (PDF) 23 желтоқсан 2015 ж. Алынған 20 қыркүйек 2015.
- ^ Xu, W-H.; Pyykkö, P. (2016). "Is the chemistry of lawrencium peculiar?" (PDF). Физикалық химия Химиялық физика. 18 (26): 17351–17355. Бибкод:2016PCCP...1817351X. дои:10.1039/C6CP02706G. hdl:10138/224395. PMID 27314425.
- ^ а б Greenwood and Earnshaw
- ^ а б King, R. B. (1995). Inorganic Chemistry of Main Group Elements. Нью-Йорк: Вили-ВЧ. б. 289. ISBN 978-1-56081-679-9.
- ^ Гринвуд және Эрншоу, б. 958
- ^ Гринвуд және Эрншоу, б. 947
- ^ Гринвуд және Эрншоу, б. 957
- ^ Коннелли, Н.Г .; Damhus, T.; Hartshorn, R. M.; Hutton, A. T. (2005). Бейорганикалық химия номенклатурасы: IUPAC ұсынымдары 2005 ж (PDF). RSC Publishing. б. vii. ISBN 978-0-85404-438-2. Мұрағатталды (PDF) түпнұсқадан 2018 жылғы 23 қарашада. Алынған 26 қараша 2018.
Lesser omissions include ... the several different outdated versions of the periodic table. (That on the inside front cover is the current IUPAC-agreed version.)
- ^ Leigh, G. J. (2009). "Periodic Tables and IUPAC". Халықаралық химия. 31 (1). дои:10.1515/ci.2009.31.1.4. Мұрағатталды түпнұсқадан 2018 жылғы 27 қарашада. Алынған 27 қараша 2018.
- ^ Дженсен, Уильям Б. (2008). "The Periodic Table: Facts or Committees?". Химиялық білім журналы. 85 (11): 1491–2. Бибкод:2008JChEd..85.1491J. дои:10.1021/ed085p1491.2.
- ^ Scerri, P.; Parsons, B. (2018). "What elements belong in group 3 of the Periodic Table?". Скерриде, Е .; Restrepo, G. (ред.) Менделеевтен Оганессонға дейін: Периодтық жүйедегі көпсалалы перспектива. Нью-Йорк: Оксфорд университетінің баспасы. 140–151 бет. ISBN 978-0-190-66853-2.
- ^ Lee, J. D. (1996). Concise inorganic chemistry (5-ші басылым). Oxford: Blackwell-Science. б. 679. ISBN 978-0-6320-5293-6.
- ^ Barbalace, Kenneth. «Элементтердің периодтық жүйесі». Environmental Chemistry.com. Алынған 2007-04-14.
- ^ Bernhard, F. (2001). "Scandium mineralization associated with hydrothermal lazurite-quartz veins in the Lower Austroalpie Grobgneis complex, East Alps, Austria". Mineral Deposits in the Beginning of the 21st Century. Лиссе: Балкема. ISBN 90-265-1846-3.
- ^ а б Kristiansen, Roy (2003). "Scandium – Mineraler I Norge" (PDF). Штайн (in Norwegian): 14–23. Архивтелген түпнұсқа (PDF) 2010 жылғы 8 қазанда.
- ^ von Knorring, O.; Condliffe, E. (1987). "Mineralized pegmatites in Africa". Геологиялық журнал. 22: 253. дои:10.1002/gj.3350220619.
- ^ Ствертка, Альберт (1998). «Итрий». Элементтерге арналған нұсқаулық (Қайта қаралған ред.) Оксфорд университетінің баспасы. бет.115–116. ISBN 0-19-508083-1.
- ^ Hedrick, James B. "Rare-Earth Metals" (PDF). USGS. Алынған 2009-06-06.
- ^ Castor, Stephen B.; Hedrick, James B. "Rare Earth Elements" (PDF). Алынған 2009-06-06.
- ^ "Mineral Commodity Summaries 2010: Yttrium" (PDF). Америка Құрама Штаттарының геологиялық қызметі. Алынған 2011-07-07.
- ^ Эмсли 2001 ж, б. 241
- ^ а б Deschamps, Y. "Scandium" (PDF). mineralinfo.com. Архивтелген түпнұсқа (PDF) 2009 жылғы 25 ақпанда. Алынған 2008-10-21.
- ^ "Mineral Commodity Summaries 2010: Scandium" (PDF). Америка Құрама Штаттарының геологиялық қызметі. Алынған 2011-07-07.
- ^ а б Холлеман, Арнольд Ф.; Wiberg, Egon; Wiberg, Nils (1985). Lehrbuch der Anorganischen Chemie (неміс тілінде) (91-100 ред.). Вальтер де Грюйтер. 1056–1057 беттер. ISBN 3-11-007511-3.
- ^ а б c Lenntech (1998). "Scandium (Sc) — chemical properties of scandium, health effects of scandium, environmental effects of scandium". Леннтех. Алынған 2011-05-21.
- ^ Макдональд, Н.С .; Нусбаум, Р. Е .; Александр, Г.В. (1952). «Итрийдің қаңқа тұнбасы» (PDF). Биологиялық химия журналы. 195 (2): 837–841. PMID 14946195.
- ^ а б c Эмсли 2001 ж, 495-498 беттер
- ^ а б c Эмсли 2001 ж, б. 240
- ^ Pol, Arjan; Барендс, Томас Р. М .; Dietl, Andreas; Хадем, Ахмад Ф .; Эйгенштейн, Джель; Джеттен, Майк С.М .; Op Den Camp, Huub J. M. (2013). «Жердің сирек металдары вулкандық батпақтардағы метанотрофтық өмір үшін өте маңызды». Экологиялық микробиология. 16 (1): 255–64. дои:10.1111/1462-2920.12249. PMID 24034209.
Библиография
- Эмсли, Джон (2001). Табиғаттың құрылыс материалдары: элементтерге арналған A-Z нұсқаулығы. АҚШ: Оксфорд университетінің баспасы. ISBN 0-19-850341-5.