WikiDer > Кальций ацетаты - Википедия
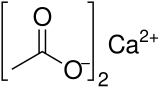 | |
 Кальций ацетаты кристалдары | |
| Атаулар | |
|---|---|
| IUPAC атауы Кальций ацетаты | |
| Басқа атаулар Әк ацетаты Кальций этанаты Кальций диацетаты | |
| Идентификаторлар | |
3D моделі (JSmol) | |
| Қысқартулар | Ca (OAc)2 |
| 3692527 | |
| Чеби | |
| ЧЕМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA ақпарат картасы | 100.000.492 |
| EC нөмірі |
|
| E нөмірі | E263 (консерванттар) |
| 22320 | |
| KEGG | |
PubChem CID | |
| RTECS нөмірі |
|
| UNII | |
CompTox бақылау тақтасы (EPA) | |
| |
| |
| Қасиеттері | |
| C4H6CaO4 | |
| Молярлық масса | 158.166 г · моль−1 |
| Сыртқы түрі | Ақ қатты гигроскопиялық |
| Иіс | шамалы сірке қышқылы иіс |
| Тығыздығы | 1,509 г / см3 |
| Еру нүктесі | 160 ° C (320 ° F; 433 K)[1] CaCO дейін ыдырау3 + ацетон |
| 37,4 г / 100 мл (0 ° C) 34,7 г / 100 мл (20 ° C) 29,7 г / 100 мл (100 ° C) | |
| Ерігіштік | аздап ериді метанол, гидразин ерімейді ацетон, этанол және бензол |
| Қышқылдық (бҚа) | шамамен 0.7 |
| -70.7·10−6 см3/ моль | |
Сыну көрсеткіші (nД.) | 1.55 |
| Фармакология | |
| V03AE07 (ДДСҰ) | |
| Қауіпті жағдайлар | |
| NFPA 704 (от алмас) | |
| 680 - 730 ° C (1,256 - 1,346 ° F; 953 - 1003 K) | |
| Өлтіретін доза немесе концентрация (LD, LC): | |
LD50 (медианалық доза) | 4280 мг / кг (ауызша, егеуқұйрық) |
| Байланысты қосылыстар | |
Басқа катиондар | Магний ацетаты |
Өзгеше белгіленбеген жағдайларды қоспағанда, олар үшін материалдар үшін деректер келтірілген стандартты күй (25 ° C [77 ° F], 100 кПа). | |
| Infobox сілтемелері | |
Кальций ацетаты Бұл химиялық қосылыс бұл а кальций тұз туралы сірке қышқылы. Онда Ca (C) формуласы бар2H3O2)2. Оның стандартты атауы - кальций ацетаты, ал кальций этанаты деген жүйелі атау. Ескі есім әк ацетаты. The сусыз формасы өте жақсы гигроскопиялық; сондықтан моногидрат (Ca (CH3COO)2• H2O) - бұл қарапайым форма.
Өндіріс
Кальций ацетатын сіңдіру арқылы дайындауға болады кальций карбонаты (жұмыртқа қабығында немесе сияқты қарапайым карбонатты жыныстарда кездеседі әктас немесе мәрмәр) немесе сіркедегі гидратталған әк:
- CaCO3(-тер) + 2CH3COOH (ақ) → Ca (CH3COO)2(aq) + H2O (l) + CO2(ж)
- Ca (OH)2(-тер) + 2CH3COOH (ақ) → Ca (CH3COO)2(aq) + 2H2O (l)
Екі реактив те бұрын қол жетімді болғандықтан, химиялық зат сол кезде кристалл ретінде бақыланған болар еді.
Қолданады
- Жылы бүйрек ауруы, қанның деңгейі фосфат көтерілуі мүмкін (деп аталады гиперфосфатемия) сүйек проблемаларына алып келеді. Кальций ацетаты қандағы фосфат деңгейін төмендету үшін тамақ құрамындағы фосфатты байланыстырады.[2]
- Кальций ацетаты а ретінде қолданылады тамақ қоспасы, тұрақтандырғыш ретінде, буфер және секвестрант, негізінен E263 нөмірі бойынша кәмпит өнімдерінде.
- Тофу дәстүрлі түрде коагуляциялау арқылы алынады Соя сүті бірге кальций сульфаты. Кальций ацетаты жақсы балама болып табылды; еритін болғандықтан, ол аз шеберлікті және аз мөлшерді қажет етеді.[3]
- Кальций ацетаты арзан болғандықтан, синтездеу үшін қарапайым бастапқы зат болған ацетон дамуына дейін кумен процесі:[4][5]
- Ca (CH3COO)2 → CaCO3(-тер) + (CH3)2CO
- Кальций ацетатының алкогольдегі қаныққан ерітіндісі жартылай қатты, тез тұтанатын гель түзеді, ол «консервіленген жылу» сияқты өнімдерге өте ұқсас. Штерно.[6] Химия пәнінің мұғалімдері кальций ацетаты ерітіндісінің қоспасы мен «Калифорния снежинкаларын» жиі дайындайды этанол.[7] Алынған гельдің түсі ақшыл және оны а-ға ұқсас етіп жасауға болады қар.
Табиғи құбылыс
Таза Са ацетаты минералдар арасында әлі белгісіз. Кальцлазит - кальций ацетаты хлорид пентаидраты белгілі минералдар тізіміне енгізілген, бірақ оның генезисі антропогендік болуы мүмкін және ол жақын арада беделін түсіруі мүмкін.[8][9]
Әдебиеттер тізімі
- ^ Дейл Л.Перри (19 мамыр, 2011). Бейорганикалық қосылыстар туралы анықтама (Екінші басылым). Тейлор және Фрэнсис. б. 84. ISBN 978-1-4398-1461-1.
- ^ «Кальций ацетаты». Mayo клиникасы. Алынған 19 қараша 2019.
- ^ Джу Лу, Элоиз Картер және Р.А.Чунг (1980): «Кальций тұздарын соя сүзбесін дайындау үшін қолдану» Food Science журналы, 45 том, 1 шығарылым, 32–34 беттер дои:10.1111 / j.1365-2621.1980.tb03864.x
- ^ Лео Фрэнк Гудвин; Эдвард Тиге Стерн (1920). «Әк ацетатын дистилляциялау арқылы ацетонды дайындаудағы шығындар». Өндірістік және инженерлік химия. 12 (3): 240–243. дои:10.1021 / ie50123a012.
- ^ Ардаг; A. D. Barbour; Г.Э. Макклеллан; Э.В.Мкбрайд (1924). «Әк ацетатын айдау». Өндірістік және инженерлік химия. 16 (11): 1133–1139. дои:10.1021 / ie50179a013.
- ^ Химиялық білім беру журналындағы «Консервіленген жылу» «Химия тіріледі!»
- ^ Химияны оқытудың ресурстары
- ^ https://www.mindat.org/min-862.html
- ^ https://www.ima-mineralogy.org/Minlist.htm
