WikiDer > Ниобий диоксиді
 | |
| Атаулар | |
|---|---|
| IUPAC атауы ниобий (IV) оксиді, ниобий диоксиді | |
| Басқа атаулар ниобий (IV) оксиді, колумбий диоксиді | |
| Идентификаторлар | |
3D моделі (JSmol) | |
| ECHA ақпарат картасы | 100.031.632 |
| EC нөмірі |
|
PubChem CID | |
CompTox бақылау тақтасы (EPA) | |
| |
| |
| Қасиеттері | |
| NbO2 | |
| Молярлық масса | 124,91 г / моль |
| Сыртқы түрі | көкшіл қара қатты |
| Еру нүктесі | 1,915 ° C (3,479 ° F; 2,188 K)[1] |
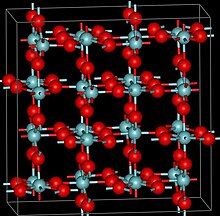
| Құрылым | |
| Тетрагональ, tI96 | |
| I41/ а, №88 | |
Өзгеше белгіленбеген жағдайларды қоспағанда, олар үшін материалдар үшін деректер келтірілген стандартты күй (25 ° C [77 ° F], 100 кПа). | |
| Infobox сілтемелері | |
Ниобий диоксиді, болып табылады химиялық қосылыс бірге формула NbO2. Бұл көкшіл-қара стехиометриялық емес NbO құрамы бар қатты1.94-NbO2.09.[1] Оны Nb азайту арқылы дайындауға болады2O5 Н2 800-1350 ° C температурада.[1] Баламалы әдіс - реакция Nb2O5 1100 ° C температурасында Nb ұнтағымен.[2]
Қасиеттері
NbO бөлме температурасының формасы2 бар төртбұрышты, рутил- Nb-Nb байланысын көрсететін қысқа Nb-Nb арақашықтықтары бар құрылым тәрізді.[3] Жоғары температура формасында а рутил- қысқа Nb-Nb арақашықтықтары бар құрылым тәрізді.[4] Екі жоғары қысымды фаза рутил тәрізді құрылыммен, қайтадан Nb-Nb қашықтықпен және одан жоғары қысыммен бадделейит- байланысты құрылым[5]
NbO2 суда ерімейді және қалпына келтіретін күшті тотықсыздандырғыш Көмір қышқыл газы көміртекке және күкірт диоксиді күкіртке дейін.[1] Ниобий металын алуға арналған өндірістік процесте NbO2 сутегінің тотықсыздануымен аралық ретінде өндіріледі Nb2O5.[6] NbO2 кейіннен магний буымен реакцияға түсіп, ниобий металын алады.[7]
Әдебиеттер тізімі
- ^ а б c г. C. K. Gupta, A. K. Suri, S Gupta, K Gupta (1994), Ниобийдің өндіруші металлургиясы, CRC Press, ISBN 0-8493-6071-4
- ^ Прадёт Патнаик (2002), Бейорганикалық химиялық заттар туралы анықтама, McGraw-Hill Professional, ISBN 0-07-049439-8
- ^ Уэллс А.Ф. (1984) Құрылымдық бейорганикалық химия 5-ші шығарылым Oxford Science Publications ISBN 0-19-855370-6
- ^ Болзан, А; Фонг, Селеста; Кеннеди, Брендан Дж .; Ховард, Кристофер Дж. (1994). «Жартылай өткізгіштік пен металдың ниобий диоксидінің нейтронды дифракциясын зерттеу». Қатты күйдегі химия журналы. 113 (1): 9–14. Бибкод:1994JSSCh.113 .... 9B. дои:10.1006 / jssc.1994.1334.
- ^ Хейнс, Дж .; Легер, Дж. М .; Перейра, A. S. (1999). «Ниобий диоксидінің жартылай өткізгіштегі жоғары қысымды құрылымдық фазалық ауысулары». Физикалық шолу B. 59 (21): 13650. Бибкод:1999PhRvB..5913650H. дои:10.1103 / PhysRevB.59.13650. hdl:10183/198788.
- ^ Патент EP1524252, ниобий субоксиді негізінде жасалған күйдірілген денелер, Schnitter C, Wötting G
- ^ Тантал / ниобий металл ұнтақтарын олардың оксидтерін газ тәрізді магниймен тотықсыздандыру арқылы алу әдісі, 6171363 АҚШ патенті, Шехтер Л.Н., Трипп Т.Б., Ланин Л.Л. (H. C. Starck, Inc.)