WikiDer > Күкірт диоксиді
 | |
 | |
| Атаулар | |
|---|---|
| Басқа атаулар күкірт (II) оксиді SO dimer | |
| Идентификаторлар | |
3D моделі (JSmol) | |
| |
| |
| Қасиеттері | |
| S2O2 | |
| Молярлық масса | 96,1299 г / моль |
| Сыртқы түрі | газ |
| Құрылым | |
| иілген | |
| Қауіпті жағдайлар | |
| Негізгі қауіптер | улы |
| Байланысты қосылыстар | |
Байланысты қосылыстар | тетрасүкірт СО, S3O S2O |
Өзгеше белгіленбеген жағдайларды қоспағанда, олар үшін материалдар үшін деректер келтірілген стандартты күй (25 ° C [77 ° F], 100 кПа). | |
| Infobox сілтемелері | |
Күкірт диоксиді, димерлі күкірт тотығы немесе SO dimer болып табылады оксид туралы күкірт формуласымен S2O2.[2] Қатты дене температурасы бірнеше секунд ішінде тұрақсыз.[3]
Құрылым
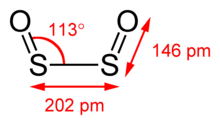
Күкірт диоксиді а cis жазықтық құрылымымен C2v симметрия. S − O байланысының ұзындығы 145,8 сағ, қарағанда қысқа күкірт тотығы. S − S байланысының ұзындығы 202.45 pm, ал O − S − S бұрышы 112.7 °. S2O2 диполь моменті 3,17 D құрайды.[4] Бұл асимметриялық жоғарғы молекула.[1][5]
Қалыптасу
Күкірт тотығы (SO) күкірт диоксидіне айналады (S2O2) өздігінен және қайтымды.[4] Сонымен, затты күкірт тотығын өндіретін әдістермен жасауға болады. Күкірт диоксиді электр разрядынан пайда болған күкірт диоксиді.[5] Зертхананың тағы бір процедурасы - оттегі атомдарын реакцияға қосу карбонилсульфид немесе көміртекті дисульфид бу.[6]
Элементтік күкірттің көптеген формалары болғанымен (S8 және басқа сақиналар мен тізбектер) SO-мен біріктірілмейді2, атомдық күкірт күкірт тотығын түзеді, ол азаяды:[7]
- S + SO2 → С.2O2 SO 2 SO
Күкірт диоксиді сондай-ақ сұйылтылған күкірт диоксидіндегі микротолқынды пеште шығарылады гелий.[8] 0,1 мм рт.ст. қысымда (13 Па) нәтиженің бес пайызы S құрайды2O2.[9]
Күкірт диоксиді уақытша пайда болады күкіртті сутек және оттегі өтеді жарқыл фотолизі.[10]
Қасиеттері
The иондану энергиясы күкірт диоксидінің 9.93±0,02 эВ.[6]
Күкірт диоксиді, байқалғандай, 320-400 нм-де сіңеді Венералық атмосфера,[11] және ықпал етті деп саналады парниктік әсер сол планетада.[12]
Реакциялар
Күкірт диоксиді тепе-теңдікте болғанымен күкірт тотығы, ол түзілу үшін күкірт тотығымен әрекеттеседі күкірт диоксиді және күкірт тотығы.[8][13]
Кешендер
S2O2 болуы мүмкін лиганд өтпелі металдармен. Ол байланыстырады η2Күкірт атомдарының екеуі де атом атомымен байланысқан -S – S позициясы.[14] Бұл алғаш рет 2003 жылы көрсетілген. Бис (триметилфосфин) тииран S-оксид кешені платинажылыту кезінде толуол 110 ° C температурада жоғалады этилен, және S-мен кешен құрайды2O2: (Ph3P)2Pt (S2O2).[15] Иридиум атомдар сонымен қатар кешен құра алады: cis- [(dppe)2IRS2] Cl натрий периодаты тотықтырады [(dppe)2IRS2O], содан кейін [(dppe) дейін2IRS2O2], dppe болуымен 1,2-бис (дифенилфосфино) этан.[16][17] Бұл затта S бар2O2 ішінде cis позиция. Дәл осындай жағдайлар а транс күрделі, бірақ бұл екі бөлек СО орнына радикалдар. Иридий кешенін ыдыратуға болады трифенилфосфин қалыптастыру трифенилфосфин оксиді және трифенилфосфин сульфиді.[16]
Анион
The S
2O−
2 анион газ фазасында байқалды. Ол қабылдауы мүмкін тригоналды ұқсас пішін СО3.[18]
Спектр
Микротолқынды пеш
| Өтпелі кезең | Жиілік (МГц)[5] |
|---|---|
| 21,1−20,2 | 11013.840 |
| 41,3−40,4 | 14081.640 |
| 11,1−00,0 | 15717.946 |
| 40,4−31,3 | 16714.167 |
| 31,3−20,2 | 26342.817 |
| 42,2−41,3 | 26553.915 |
| 22,0−21,1 | 28493.046 |
| 60,6−51,5 | 30629.283 |
| 52,4−51,5 | 35295.199 |
| 51,5−40,4 | 35794.527 |
Күн жүйесінде
Күкірт диоксиді құрамында кішкене компонент болуы мүмкін екендігінің бірнеше дәлелі бар Венераның атмосферасыжәне бұл планетаның қатты әсер етуі мүмкін парниктік әсер.[11] Ол Жер атмосферасында ешқандай маңызды мөлшерде кездеспейді.
Әдебиеттер тізімі
- ^ а б Демейсон, Жан; Фогт, Юрген (2011). «836. О2S2 Күкірт диоксиді « (PDF). Асимметриялық жоғарғы молекулалар, 3 бөлім. Ландолт-Борнштейн: II топ молекулалары мен радикалдары. 29D3. Спрингер. б. 492. дои:10.1007/978-3-642-14145-4_258. ISBN 9783642141454.
- ^ Холлеман, Арнольд Ф.; Wiber, Эгон; Wiberg, Nils, редакциялары. (2001). «Күкірт оксидтері». Бейорганикалық химия. Академиялық баспасөз. б. 530. ISBN 9780123526519.
- ^ Митчелл, Стивен С. (2004). Күкірт қосылыстарының биологиялық өзара әрекеттесуі. CRC Press. б. 7. ISBN 9780203362525.
- ^ а б Lovas, F. J. (1974). «СО-ны спектроскопиялық зерттеу2 ағызу жүйесі. II. SO димерінің микротолқынды спектрі ». Химиялық физика журналы. 60: 5005. дои:10.1063/1.1681015.
- ^ а б c Торвирт, Свен; Туле, П .; Готлиб, С .; Мюллер, H. S. P .; МакКарти, М. С .; Таддеус, П. (2006). «S-нің айналмалы спектроскопиясы2O: діріл спутниктері, 33S изотопомерлер және субмиллиметрлік толқын спектрі » (PDF). Молекулалық құрылым журналы. 795 (1–3): 219–229. Бибкод:2006JMoSt.795..219T. дои:10.1016 / j.molstruc.2006.02.055.
- ^ а б Ченг, Бинг-Мин; Хунг, Вен-Чин (1999). «S-дің иондану энергиясы мен спектрі фотоотизация тиімділігі2O2". Химиялық физика журналы. 110 (1): 188. Бибкод:1999JChPh.110..188C. дои:10.1063/1.478094. ISSN 0021-9606.
- ^ Мураками, Йошинори; Ониши, Шуичи; Кобаяси, Такаоми; Фудзии, Нобуйуки; Исшики, Нобуясу; Цучия, Кентаро; Тезаки, Атсуму; Мацуи, Хироюки (2003). «S + SO жоғары температуралық реакциясы2 → SO + SO: S импликациясы2O2 Аралық кешенді қалыптастыру ». Физикалық химия журналы А. 107 (50): 10996–11000. Бибкод:2003JPCA..10710996M. дои:10.1021 / jp030471i. ISSN 1089-5639.
- ^ а б Өріс, Т.А .; Слатери, А. Е .; Адамс, Дж .; Моррисон, Д.Д (2005). «S-ге диссоциативті электрондардың қосылуын эксперименттік бақылау2O және S2O2 тұрақсыз молекулаларға арналған жаңа спектрометрмен » (PDF). Физика журналы В: Атомдық, молекулалық және оптикалық физика. 38 (3): 255–264. Бибкод:2005JPhB ... 38..255F. дои:10.1088/0953-4075/38/3/009. ISSN 0953-4075. Архивтелген түпнұсқа (PDF) 2015-09-24. Алынған 2013-05-13.
- ^ Саху, Баларам; Наяк, Нимай Чаран; Самантарай, Асутош; Пуджапанда, Прафулла Кумар (2012). Бейорганикалық химия. PHI оқыту. б. 461. ISBN 9788120343085. Алынған 2013-05-16.
- ^ Комптон, Р.Г .; Бэмфорд, C. Х .; Типпер, C. F. H. (1972). «Н тотығуы2S «. Металл емес бейорганикалық қосылыстардың реакциялары. Кешенді химиялық кинетика. Elsevier. б. 50. ISBN 9780080868011.
- ^ а б Франдсен, Б. Н .; Венберг, П. О .; Kjærgaard, H. G. (2016). «OSSO-ны Венера атмосферасындағы ультрафиолетке жақын сіңіргіш ретінде анықтау» (PDF). Геофизикалық зерттеу хаттары. 43 (21): 11146–11155. Бибкод:2016GeoRL..4311146F. дои:10.1002 / 2016GL070916.
- ^ «Венерадағы сирек молекула планетаның ауа-райын түсіндіруге көмектеседі». CBC жаңалықтары. Алынған 2016-11-11.
- ^ Херрон Дж. Т .; Huie, R. E. (1980). «SO + SO + M → (SO) реакциялары үшін жылдамдықтың тұрақтылығы 298 К2 + M және SO + (SO)2 → SO2 + С.2O «. Химиялық физика хаттары. 76 (2): 322–324. Бибкод:1980CPL .... 76..322H. дои:10.1016/0009-2614(80)87032-1.
- ^ Хэлкроу, Малкольм А .; Хафман, Джон С .; Кристу, Джордж (1994). «Жаңа S синтезі, сипаттамасы және молекулалық құрылымы2O кешені Mo (S2O) (С.2CNEt2)3·1⁄2Et2О « (PDF). Бейорганикалық химия. 33 (17): 3639–3644. дои:10.1021 / ic00095a005. ISSN 0020-1669.
- ^ Лоренц, Инго-Питер; Кулл, Юрген (1986). «Тииранды бөлшектеу кезінде күкірт диоксидін кешенді тұрақтандыру S-Бис (трифенилфосфан) платинадағы оксид (0) «. Angewandte Chemie International Edition ағылшын тілінде. 25 (3): 261–262. дои:10.1002 / anie.198602611. ISSN 0570-0833.
- ^ а б Шмид, Гюнтер; Риттер, Гюнтер; Дебаердемаекер, Тони (1975). «Die Komplekschemie niederer Schwefeloxide. II. Schwefelmonoxid und Dischwefeldioxid als Kompleksliganden» [Төменгі күкірт оксидтерінің күрделі химиясы. II. Күкірт тотығы және күкірт диоксиді күрделі лигандтар ретінде]. Химище Берихте. 108 (9): 3008–3013. дои:10.1002 / сбер.19751080921. ISSN 0009-2940.
- ^ Нагата, К .; Такеда, Н .; Tokitoh, N. (2003). «Платинаның дихалькогенидо кешендерінің әдеттен тыс тотығуы». Химия хаттары. 32 (2): 170–171. дои:10.1246 / cl.2003.170. ISSN 0366-7022.
- ^ Клементс, Тодд Г .; Ханс-Юрген Дейерл; Роберт Э. Континетти (2002). «Диссоциативті фотодеректердің динамикасы S
2O−
2" (PDF). Физикалық химия журналы А. 106 (2): 279–284. Бибкод:2002JPCA..106..279C. дои:10.1021 / jp013329v. ISSN 1089-5639. Алынған 2013-05-13.