WikiDer > ДНҚ вакцинасы
Осы мақаланың тақырыбын өзгерту туралы өтініш ДНҚ иммунизациясы болып табылады талқыланып жатыр. өтінемін Қозғалма бұл мақала талқылау жабылғанға дейін. |
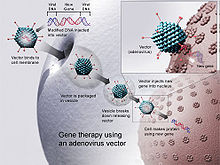
ДНҚ вакцинасы әдістемесі болып табылады трансфекциялау иммунизацияланған түрдің жасушаларына антигеннің ДНҚ кодтауының бірізділігі.[1][2]
ДНҚ вакциналары инъекция арқылы аурудан қорғайды генетикалық тұрғыдан жасалған плазмида құрамында ДНҚ кодтайтын реттілік антиген(-дер) иммундық жауап ізделетіндіктен, жасушалар антигенді түзіп, қорғаныс тудырады иммунологиялық жауап.[3] ДНҚ вакциналарының әдеттегіден теориялық артықшылықтары бар вакциналариммундық жауап түрлерінің кең спектрін шақыру қабілетін қоса.[дәйексөз қажет] Бірнеше ДНҚ вакциналары сыналды ветеринариялық пайдалану.[3] Кейбір жағдайларда жануарлардың ауруларынан қорғаныс, ал басқаларында жоқ.[3] 2016 жылдың тамыз айынан бастап АҚШ-та ДНҚ-ға қарсы вакциналар адам қолдануы үшін мақұлданбаған.[4] Жақындауға бағытталған зерттеулер жалғасуда вирустық, бактериалды және паразиттік адамдардағы аурулар, сондай-ақ бірнеше қатерлі ісік аурулары.[дәйексөз қажет]
Тарих
ДНҚ вакциналары «үшінші буын вакциналары» деп аталады. «Жүз жылдан астам уақыт ішінде вакцинацияға екі тәсілдің бірі әсер етті: немесе нақты енгізу антигендер оған қарсы иммундық жүйе тікелей реакция жасайды немесе тірі әлсіреген инфекциялық қоздырғыштарды енгізеді, олар ауру тудырмай иесінің ішінде көбейеді [және иммундық жүйені кейіннен түзетін антигендерді синтездей алады ».[3] «Жақында вакцинацияға түбегейлі жаңа тәсіл жасалды».[3]
ДНҚ вакциналарында патогеннің арнайы белоктарын (антигендерін) кодтайтын ДНҚ бар. ДНҚ денеге енгізіліп, оны қалыпты метаболизм процестері өздері қабылдаған плазмида генетикалық код негізінде синтездейтін жасушалар алады. Бұл протеиндерде амин қышқылдарының бірізділіктерінің бактериялар мен вирустарға тән аймақтары болғандықтан, олар бөгде деп танылады және оларды иесі жасушалар өңдеп, олардың бетіне шығарған кезде иммундық жүйе ескертіледі, содан кейін иммундық жауаптар пайда болады.[5][6] Сонымен қатар, ДНҚ жасушаның енуін жеңілдету үшін ақуызға салынуы мүмкін. Егер бұл капсид ақуыз ДНҚ-ға енгізілген, нәтижесінде пайда болған вакцина тірі вакцинаның күшін реверсия қаупінсіз біріктіре алады.
1983 жылы, Энцо Паолетти және Деннис Паникали Нью-Йорк денсаулық сақтау департаменті өндіру стратегиясын ойлап тапты рекомбинантты ДНҚ кәдімгі түрлендіру үшін гендік инженерияны қолдану арқылы вакциналар аусылға қарсы вакцина басқа аурулардың алдын алуға болатын вакциналарға.[7] Олар ДНҚ-ны өзгертті сиыр басқа вирустардан генді енгізу арқылы вирус (атап айтқанда Герпес қарапайым вирусы, гепатит В және тұмау).[8][9] 1993 жылы Джеффри Улмер және оның әріптестері Merck зерттеу зертханалары тұмау антигенін кодтайтын плазмидті ДНҚ-мен тышқандарды тікелей инъекциялау жануарларды тұмау вирусының кейінгі тәжірибелік инфекциясынан қорғағанын көрсетті[10]. 2016 жылы ДНҚ вакцинасы Зика вирусы бастап адамдарда сынау басталды Ұлттық денсаулық сақтау институттары. Зерттеуге 18 мен 35 жас аралығындағы 120 субъектіні тарту жоспарланған болатын. Бөлек, Inovio фармацевтика және GeneOne Life Science Майамиде Зикаға қарсы басқа ДНҚ вакцинасының сынақтарын бастады. NIH вакцинасы жоғарғы қолға жоғары қысыммен енгізіледі. 2016 жылғы тамыздағы көлем бойынша вакциналарды өндіру шешілмеген.[4] АИТВ-ның алдын алу үшін ДНҚ вакциналарына клиникалық зерттеулер жүргізілуде.[11]
Қолданбалар
Құрама Штаттарда ДНҚ-ға қарсы вакциналар адамды қолдануға рұқсат етілмеген. Бірнеше эксперименттік сынақтар аурудан қорғану үшін жеткілікті күшті реакцияны тудырды және техниканың пайдалылығы адамдарда дәлелденеді. A ветеринариялық Қорғайтын ДНҚ вакцинасы жылқылар бастап Батыс Ніл вирусы мақұлданды.[12][13]Даму құралы ретінде ДНҚ иммунизациясы да зерттелуде антивеном сарысулар.[14] ДНҚ иммунизациясын технологиялық платформа ретінде пайдалануға болады моноклоналды антидене индукция.[15]
Артықшылықтары
- Инфекция қаупі жоқ[6]
- Екі антигеннің презентациясы MHC класы I және II сынып молекулалар[6]
- Т-жасушаның реакциясын 1 типке немесе 2 типке поляризациялаңыз[6]
- Иммундық жауап қызығушылықтың антигеніне бағытталған
- Даму мен өндірудің қарапайымдылығы[6]
- Сақтау және тасымалдау үшін тұрақтылық
- Экономикалық тиімділік
- Пептидті синтездеу, рекомбинантты ақуыздарды экспрессиялау және тазарту және улы адъюванттарды қолдану қажеттілігін жояды[16]
- Иммуногеннің ұзақ мерзімді тұрақтылығы[5]
- In vivo экспрессия ақуыздың қалыпты эукариоттық құрылымға көбірек ұқсайтындығына кепілдік береді, бұл ретте трансплантациядан кейінгі модификация жүреді[5]
Жағымсыз әсерлер
- Ақуыз иммуногендерімен шектелген (бактериялық полисахаридтер сияқты ақуыз емес антигендер үшін пайдалы емес)
- Жасушалардың өсуін басқаратын гендерге әсер ету қаупі[дәйексөз қажет]
- ДНҚ-ға қарсы антидене өндірісін индукциялау мүмкіндігі
- Өндірілген антигенге (ақуызға) төзімділік мүмкіндігі
- Бактериялардың және паразиттердің ақуыздарын атипті өңдеу мүмкіндігі[6]
- Ми жасушалары сияқты мақсатты емес жасушаларды трансфекциялау үшін плазмидалық ДНҚ нанобөлшектерін мұрынға бүрку әдісін қолдану мүмкіндігі[17]
Плазмидалық векторлар
Векторлық дизайн
ДНҚ вакциналары жоғары белсенді экспрессия векторларын қолданған кезде ең жақсы иммундық жауап береді. Бұлар плазмидалар in vivo-ны басқаратын күшті вирустық промотордан тұратын әдетте транскрипция және аударма геннің (немесе комплементарлы ДНҚ) қызығушылық.[18] Intron A жетілдіру үшін кейде енгізілуі мүмкін мРНҚ тұрақтылық, демек ақуыздың экспрессиясын жоғарылатады.[19] Плазмидаларға күшті де жатады полиаденилдеу/ сиыр сияқты транскрипциялық тоқтату сигналы өсу гормоны немесе қоян бета-глобулин полиаденилдену реттілігі.[5][6][20] Поликистроникалық векторлар (бірнеше геном учаскелерінде орналасқан) кейде бірнеше иммуногенді шығару үшін немесе иммуноген мен иммуностимуляторлы ақуызды экспрессиялау үшін құрылады.[21]
Плазмида иммуногеннің экспрессияланатын «құралы» болғандықтан, ақуыздың максималды экспрессиясына арналған векторлық дизайнды оңтайландыру қажет.[21] Ақуыздың экспрессиясын жақсартудың бір әдісі - оңтайландыру кодон патогенді мРНҚ-ны қолдану эукариоттық жасушалар. Қоздырғыштар әр түрлі болады AT-мазмұны мақсатты түрлерге қарағанда, сондықтан гендер тізбегі иммуногеннің көрінуі кодондар мақсатты түрлерде жиі қолданылатын оның экспрессиясын жақсартуы мүмкін.[22]
Тағы бір ескеру - таңдау промоутер. The SV40 промотор шартты түрде зерттеушілер векторлардың көмегімен қозғалатындығын көрсеткенге дейін қолданылды Rous Sarcoma вирусы (RSV) промоутерде экспрессия жылдамдығы едәуір жоғары болды.[5] Жақында экспрессия ставкалары цитомегаловирус (CMV) дереу ерте промоутер. Қосу Mason-Pfizer маймылының вирусы (MPV) -CTE бар / жоқ айн[ажырату қажет] конверт экспрессиясының жоғарылауы. Сонымен қатар, CTE + rev құрылымы CTE жалғыз векторына қарағанда айтарлықтай иммуногенді болды.[23] Экспрессия жылдамдығын жақсартуға арналған қосымша модификацияға синтетикалық күшейткіш тізбекті енгізу кіреді интрондар, аденовирус үш жақты көшбасшы (TPL) тізбегі және полиаденилдену мен транскрипциялық аяқталу реттілігінің модификациясы.[5] ДНҚ вакцина плазмидасының мысалы болып табылады pVAC, ол SV40 қолданады промоутер.
Құрылымдық тұрақсыздық құбылыстары плазмида өндірісі, ДНҚ вакцинасы және гендік терапия үшін ерекше алаңдаушылық туғызады.[24] Плазмидті магистральға қатысты аксессуарлық аймақтар құрылымдық тұрақсыздықтың көптеген құбылыстарына ұшырауы мүмкін. Генетикалық тұрақсыздықтың белгілі катализаторларына тікелей, инверттелген және тандемді қайталаулар жатады, олар көптеген коммерциялық қол жетімді клондау және экспрессия векторларында көрінеді. Демек, бөгде кодтан тыс магистральды тізбектердің қысқаруы немесе толық жойылуы мұндай оқиғалардың орын алуына бейімділікті, демек, жалпы плазмиданың рекомбиногендік әлеуетін төмендетеді.[25]
Плазмидалар механизмі
Плазмида өзін трансфекцияланған жасуша ядросына енгізгеннен кейін, шетелдік антигеннің пептидтік тізбегін кодтайды. Жасуша өзінің бетінде гистосәйкестілік кешені (MHC) класс I және II класс молекулалары бар шетелдік антигенді көрсетеді. Содан кейін антигенді ұсынатын жасуша лимфа түйіндеріне өтіп, Т-жасуша сигнал берген антиген пептидті және костимуляторлы молекуланы ұсынады, иммундық реакцияны бастайды.[26]
Вакцина салғышының дизайны
Антидене немесе цитотоксикалық Т-жасушаларының реакциясын жақсарту үшін иммуногендерді әртүрлі жасушалық бөлімдерге бағыттауға болады. Құпия немесе плазмалық мембрана-байланысты антигендер антидене реакциясын индукциялауға қарағанда тиімдірек цитозоликалық антигендер, ал цитотоксикалық Т-жасуша цитоплазмалық деградацияға антигендерді бағыттау және одан әрі ену арқылы жауаптарды жақсартуға болады негізгі гистосәйкестік кешені (MHC) I класс жолы.[6] Бұл, әдетте, қосу арқылы жүзеге асырылады N-терминал убивитин сигналдар.[27][28][29]
The конформация ақуыз антиденелердің реакцияларына әсер етуі мүмкін. «Реттелген» құрылымдар (мысалы, вирустық бөлшектер) реттелмеген құрылымдарға қарағанда тиімдірек.[30] Минигендердің жіптері (немесе MHC I класы) эпитоптар) әртүрлі патогендерден цитотоксикалық Т-жасушаларының кейбір қоздырғыштарға реакциясын жоғарылатады, әсіресе TH эпитопы енгізілген болса.[6]
Жеткізу
Жануарлардың тіндеріне ДНҚ вакциналары бірнеше әдістермен енгізілген. Екі ең танымал тәсіл 1999 жылы ДНҚ-ны инъекциялау болды тұзды: стандартты гиподермиялық инені қолдану арқылы; немесе пайдалану арқылы гендік мылтық жеткізу.[31] Аралық жылдары бірнеше басқа техникалар құжатталды.
Тұзды инъекция
Ерітіндідегі инъекция әдетте бұлшықет ішіне (IM) енгізіледі қаңқа бұлшықеті, немесе тері ішілік (ID), жасушадан тыс кеңістіктерге ДНҚ жеткізеді. Бұған 1) арқылы көмектесуге болады электропорация;[32] 2) бұлшықет талшықтарын уақытша зақымдау арқылы миотоксиндер сияқты бупивакаин; немесе 3) пайдалану арқылы гипертониялық тұзды ерітінділер немесе сахароза.[5] Бұл әдіске иммундық жауаптар ине түрін қоса факторларға әсер етуі мүмкін,[16] инені туралау, инъекция жылдамдығы, инъекция көлемі, бұлшықет түрі, алушының жас, жынысы және физиологиялық жағдайы.[5]
Ген-мылтық
Ген-мылтық жеткізу баллистикалық жолмен сіңірілген ДНҚ плазмидасын (рДНҚ) жеделдетеді алтын немесе вольфрам сығылғанды пайдаланып, мақсатты ұяшықтарға микробөлшектер гелий акселерант ретінде.[5][21]
Шырышты қабаттың жеткізілуі
Баламалар енгізілген аэрозоль жалаңаш ДНҚ-ны тамызу шырышты сияқты беттер мұрын және өкпе шырышты қабық,[21] көзге рДНҚ-ны жергілікті енгізу[33] және қынаптың шырышты қабаты.[21] Шырышты қабаттың жеткізілуіне катионды қолдану арқылы да қол жеткізілді липосома-ДНҚ препараттары,[6] биологиялық ыдырайтын микросфералар,[34][21] әлсіреген Сальмоналла,[35] Шигелла немесе Листерия ішектің шырышты қабығына ішке қабылдауға арналған векторлар[36] және рекомбинантты аденовирустық векторлар.[21]
Полимерлі көлік
Жасуша және синтетикалық бактериялардан тұратын гибридті көлік құралы полимерлер ДНҚ вакцинасын жеткізу үшін жұмысқа орналастырылды. Ан E. coli ішкі ядроның және поли (бета-амин эфирінің) сыртқы қабаты синергетикалық түрде жұмыс істейді, олар байланысты кедергілерді шешу арқылы тиімділікті жоғарылатады. антиген ұсынатын жасуша клеткалық сіңіру мен интерьеризацияны қамтитын ген беру, фагосомалық қашу және жасушаішілік жүк концентрациясы. Тышқандарда тексерілген гибридті вектор иммундық жауап тудыратыны анықталды.[37][38]
ELI иммунизациясы
ДНҚ вакцинациясының тағы бір тәсілі - бұл өрнек кітапханасы иммундау (ELI). Осы техниканы қолдана отырып, патогеннің барлық гендерін бір уақытта жіберуге болады, бұл әлсіреуі немесе өсіру қиын патогендер үшін пайдалы болуы мүмкін.[5] ELI көмегімен қандай гендер қорғаныс реакциясын тудыратынын анықтауға болады. Бұл тексерілді Микоплазма пульмонис, а murine салыстырмалы түрде аз болатын өкпе патогені геном. Жартылай экспрессиялық кітапханалар да келесі қиындықтардан қорғауды тудыруы мүмкін.[39]
Пайдалы кестелік салыстыру
| Жеткізу әдісі | ДНҚ формуласы | Мақсатты тін | ДНҚ мөлшері | |
|---|---|---|---|---|
| Парентеральды | Инъекция (гиподермиялық ине) | Тұзды ерітіндідегі сулы ерітінді | IM (қаңқа); Жеке куәлік; (IV, тері астындағы және ішілік перитонеальды, ауыспалы жетістікпен) | Үлкен мөлшерде (шамамен 100-200 мкг) |
| Ген-мылтық | ДНҚ-мен қапталған алтын моншақтар | ED (іш терісі); қынаптың шырышты қабаты; хирургиялық жолмен ашық бұлшықет және басқа органдар | Аз мөлшерде (16 нг-дан аз) | |
| Пневматикалық (реактивті) инъекция | Сулы ерітінді | ED | Өте жоғары (300 мкг дейін) | |
| Өзекті қолдану | Сулы ерітінді | Көз; ішілік | Аз мөлшерде (100 мкг дейін) | |
| Цитофетиннің көмегімен | Липосомалар (катионды); микросфералар; рекомбинантты аденовирустық векторлар; әлсіреген Шигелла вектор; аэрозолизденген катионды липид тұжырымдамалар | IM; IV (тіндерді жүйелі түрде трансфекциялау үшін); іш қуысы; ішектің шырышты қабығына ауызша иммундау; мұрын / өкпенің шырышты қабаттары | айнымалы | |
| Жеткізу әдісі | Артықшылығы | Кемшілігі |
|---|---|---|
| Бұлшықет ішіне немесе тері ішіне инъекция |
|
|
| Ген-мылтық |
|
|
| Реактивті инъекция |
|
|
| Липосома арқылы жеткізіледі |
|
|
Доза
Жеткізу әдісі тиімді иммундық реакцияны көтеру үшін қажетті дозаны анықтайды. Тұзды инъекциялар үшін 10 мкг-ден 1 мг-ға дейінгі ДНҚ-ның өзгермелі мөлшері қажет, ал гендік мылтықты жеткізу 100-ден 1000 есе аз қажет етеді.[40] Әдетте 0,2 мкг - 20 мкг қажет, дегенмен 16 нг-ға дейінгі шамалар туралы хабарланған.[5] Бұл шамалар түрлерге байланысты өзгеріп отырады. Мысалы, тышқандарға қарағанда ДНҚ-ға қарағанда шамамен 10 есе аз ДНҚ қажет приматтар.[6] Тұзды инъекцияларға көп ДНҚ қажет, себебі ДНҚ мақсатты тіннің жасушадан тыс кеңістігіне (қалыпты жағдайда бұлшықет) жеткізіледі, ол жерде физикалық кедергілерді жеңуге тура келеді (мысалы, базальды ламина және үлкен мөлшерде дәнекер тін) оны жасушалар қабылдамас бұрын, гендік мылтықты жеткізген кезде ДНҚ-ны тікелей жасушаларға айдайды / мәжбүрлейді, нәтижесінде «қалдықтар» азаяды.[5][6]
Иммундық жауап
Т-жасушаларының жауаптары
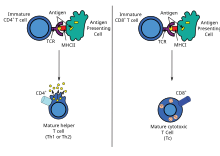
ДНҚ иммунизациясы бірнеше Т-ны көтеруі мүмкінH реакциялар, соның ішінде лимфопролиферация және алуан түрлілік цитокин профильдер. ДНҚ вакциналарының басты артықшылығы - оларды TH1 немесе TH2 реакцияларына қарай Т-жасушаларының анықтамалық түріне бейімдеу үшін манипуляциялаудың ыңғайлылығы.[41] Әр типтің ерекше заңдылықтары бар лимфокин және химокиннің экспрессиясы, спецификалық түрлері иммуноглобулиндер, лимфоциттердің айналымының заңдылықтары және түрлері туа біткен иммундық жауаптар.
Т-жасушаларының басқа түрлері
Көтерілген Т-жасушалық көмек түріне жеткізу әдісі және иммуногеннің экспрессияланған түрі, сондай-ақ әр түрлі лимфоидты бөлімдердің бағытталуы әсер етеді.[5][42] Әдетте, иненің инъекциялық инъекциясы (IM немесе ID) TH1 реакциясын тудырады, ал гендік мылтық беру TH2 реакциясын жоғарылатады.[41][42] Бұл жасушаішілік және плазмалық мембранамен байланысқан антигендерге қатысты, бірақ бөлу әдісіне қарамастан TH2 реакциясын тудыратын секрецияланған антигендерге қатысты емес.[43]
Әдетте, көтерілген Т-жасуша түрінің түрі уақыт бойынша тұрақты болып келеді және қарсылық білдіргенде немесе одан кейінгі иммунизациядан кейін өзгермейді, бұл әдеттегідей аңқау үлгіде реакцияның қарама-қарсы түрін тудыруы мүмкін.[41][42] Алайда, Мор т.б.. (1995)[18] тышқанның циркумспорозоит ақуызын кодтайтын рДНҚ-мен иммунизацияланған және күшейтілген тышқандар безгек паразит Plasmodium yoelii (PyCSP) анықтап, TH2 реакциясы TH1 жауабына дейін жоғарылағаннан кейін өзгергенін анықтады.
Т-жасушаларының әр түрлі типтегі анықтамаларының негізі
Осы әртүрлі әдістердің қалай жұмыс істейтіні, антигеннің формалары және Т-жасушаның әртүрлі профильдері анықталмаған. IM инъекциясында қолданылатын салыстырмалы түрде көп мөлшердегі ДНҚ TH1 жауаптарының индукциясы үшін жауап береді деп ойлады. Алайда, дәлелдер TH типіндегі дозаға байланысты айырмашылықтарды көрсетпейді.[41] Көтерілген Т-жасушалық анықтаманың түрі дифференциалды күйімен анықталады антигенді ұсынатын жасушалар. Дендритті жасушалар бөлуге болады ИЛ-12 (бұл TH1 жасушасының дамуын қолдайды) немесе IL-4 (бұл TH2 жауаптарын қолдайды).[44] ине арқылы енгізілген рДНҚ - бұл эндоциттелген дендритті жасушаға, содан кейін TH1 үшін дифференциалдану үшін қозғалады цитокин өндіріс,[45] гендік мылтық ДНҚ-ны тікелей жасушаға бомбалайды, осылайша TH1 стимуляциясын айналып өтеді.
Поляризацияланған Т-жасуша көмегін практикалық қолдану
Т-жасуша көмегіндегі поляризация әсер етуде пайдалы аллергиялық жауаптар және аутоиммунды аурулар. Аутоиммунды аурулар кезінде мақсат аутодеструктивті TH1 реакциясын (оның цитотоксикалық Т жасушасының белсенділігімен) бұзбайтын TH2 реакциясына ауыстыру болып табылады. Бұл клиникаға дейінгі модельдерде жауаптың қажетті түріне алдын-ала дайындық кезінде сәтті қолданылды[6] және белгілі бір аурудың реакциясын ауыстыруда сәтті.[46]
Т-жасушаларының цитотоксикалық реакциясы
ДНҚ вакциналарының артықшылықтарының бірі - олар индукциялауға қабілетті цитотоксикалық Т лимфоциттері (CTL) тірі вакциналармен байланысты тәуекелсіз. CTL реакцияларын иммунодоминантты және иммуноресессивті CTL эпитоптарына қарсы көтеруге болады,[47] сонымен қатар субдоминантты CTL эпитоптары,[34] табиғиға еліктейтін тәрізді инфекция. Бұл CTL эпитоптарын және олардың иммунитетті қамтамасыз етудегі рөлін бағалауда пайдалы құрал болуы мүмкін.
Цитотоксикалық Т-жасушалар ұсақтарды таниды пептидтер (8-10 аминқышқылдары) дейін күрделі MHC класы I молекулалар.[48] Бұл пептидтер ыдырайтын эндогендік цитозолды ақуыздардан алынады және олар MHC класының жаңа туындайтын молекуласына жеткізіледі. эндоплазмалық тор (ER).[48] Тікелей ЭР-ге гендік өнімдерді бағыттау (ан қосу арқылы амин-терминал кірістіру жүйелі) осылайша CTL жауаптарын жақсартуы керек. Бұл рекомбинантты қолдану арқылы сәтті көрсетілді вакциния вирустар тұмау ақуыздар,[48] бірақ бұл принцип ДНҚ вакциналарына да қатысты болуы керек. Қосу арқылы жасушаішілік деградацияға қарсы антигендерді (және MHC класс жолына енуді) мақсатты ету убивитин сигналдар тізбегі немесе басқа сигналдар тізбегінің мутациясы CTL жауаптарын жоғарылатуда тиімді болып шықты.[28]
CTL реакцияларын, мысалы, стимуляторлы молекулалармен бірге егу арқылы жақсартуға болады B7-1 немесе B7-2 тұмауға қарсы нуклеопротеидке қарсы ДНҚ вакциналары үшін,[47][49] немесе GM-CSF безгек моделіне қарсы ДНҚ вакциналары үшін P. yoelii.[50] Ил-12 және TCA3 ко-стимуляторлы молекулаларын кодтайтын плазмидалармен бірге егудің АИТВ-1 және тұмаудың нуклеопротеин антигендеріне қарсы CTL белсенділігін жоғарылататындығы көрсетілген.[49][51]
Гуморальды (антидене) жауап
ДНҚ-ға қарсы вакцинация нәтижесінде пайда болған антиденелердің реакцияларына көптеген айнымалылар, соның ішінде антиген типі әсер етеді; антигеннің орналасуы (яғни жасушаішілік және секрецияланған); саны, жиілігі және иммундау дозасы; антигенді жеткізу орны және әдісі.
Антидене реакциясының кинетикасы
Бір рет ДНҚ енгізгеннен кейінгі гуморальды реакциялар рекомбинантты ақуызбен бір рет енгізгеннен гөрі ұзақ өмір сүруі мүмкін. Антиденелердің жауаптары гепатит В вирустық (HBV) конверттегі ақуыз (HBsAg) 74 аптаға дейін күшеймей, тұмауға қарсы қорғаныс реакциясын өмір бойына сақтайды гемагглютинин гендік мылтық жеткізілгеннен кейін тышқандарда көрсетілді.[52] Антидене бөлетін жасушалар сүйек кемігі және көкбауыр ұзақ мерзімді антиденелерді өндіру үшін, және, әдетте, бір жылдан кейін локализациялау.[52]
Табиғи (вирустық) инфекциядан туындаған антиденелердің реакцияларын салыстыру, рекомбинантты протеинмен иммунизация және рДНҚ иммунизациясы 4-кестеде келтірілген. ДНҚ көтерілген антиденелердің жауаптары табиғи инфекция немесе рекомбинантты ақуызға қарсы иммунизация пайда болғанға қарағанда әлдеқайда баяу көтеріледі. Тышқандардағы ең жоғарғы титрларға жету үшін 12 апта қажет болуы мүмкін, дегенмен күшейту аралықты төмендетуі мүмкін. Бұл жауап антиденелер реакциясының бастапқы және қайталама фазаларын қолдайтын бірнеше апта ішінде көрсетілген антигеннің төмен деңгейіне байланысты болуы мүмкін. Созылмалы гепатиті бар ересектерге HBV шағын және орта конверттегі ақуызды көрсететін ДНҚ вакцинасы енгізілді. Вакцина спамның интерферонды гамма-жасушаларын өндіруге әкелді. Сондай-ақ орта қабықтағы антигендерге арналған арнайы Т-жасушалар жасалды. Пациенттердің иммундық реакциясы HBV инфекциясын бақылау үшін жеткіліксіз болды[53]
| Иммундау әдісі | |||
|---|---|---|---|
| ДНҚ вакцинасы | Рекомбинантты ақуыз | Табиғи инфекция | |
| Индуктивті антигеннің мөлшері | нг | мкг | ? (нг-мкг) |
| Антиген презентациясының ұзақтығы | бірнеше апта | <1 апта | бірнеше апта |
| Антидене реакциясының кинетикасы | баяу көтерілу | тез көтерілу | тез көтерілу |
| Жоғары авидтілік IgG алу үшін егулер саны және ASC-нің сүйек кемігіне көшуі | бір | екі | бір |
| Ab изотипі (мурин модельдері) | C’-тәуелді немесе C’-тәуелді емес | C’ тәуелді | C’-тәуелсіз |
Сонымен қатар, ДНҚ-ға қарсы вакцинамен көтерілген арнайы антиденелердің титрлары рекомбинантты ақуызбен вакцинациядан кейін алынғаннан төмен. Алайда, ДНҚ иммунизациясынан туындаған антиденелер рекомбинантты протеинмен туындаған антиденелерге қарағанда, жергілікті эпитоптарға жақындығын көрсетеді. Басқаша айтқанда, ДНҚ иммунизациясы сапалы жоғары реакцияны тудырады. Антиденелерді ДНҚ-мен бір вакцинациядан кейін индукциялауға болады, ал рекомбинантты ақуызға вакцинация әдетте күшейтуді қажет етеді. ДНҚ иммунизациясы иммундық жауаптың TH профилін және осылайша антидененің изотипін біржақты ету үшін қолданылуы мүмкін, бұл табиғи инфекциямен де, рекомбинантты ақуызбен иммундаумен де мүмкін емес. ДНҚ тудыратын антиденелердің реакциясы дайындық құралы ретінде пайдалы. Мысалы, реагент ретінде пайдалану үшін поликлоналды және моноклоналды антиденелерді жасауға болады.
ДНҚ көтерілген иммундық жауаптардың механикалық негіздері
ДНҚ сіңіру механизмі
ДНҚ-ны қабылдау және одан кейінгі экспрессия алғаш рет көрсетілгенде in vivo жылы бұлшықет жасушалар,[54] бұл жасушалар T-түтікшелерінің кең желісіне байланысты ерекше деп саналды. Қолдану электронды микроскопия, ДНҚ-ны қабылдауды жеңілдету ұсынылды кавеола (немесе, клатринсіз қапталған шұңқырлар).[55] Алайда, кейінгі зерттеулер басқа жасушалардың (мысалы кератиноциттер, фибробласттар және эпителий Лангерганс жасушалары) сонымен қатар ДНҚ-ны ішкі күйге келтіруі мүмкін[46][56] ДНҚ сіңіру механизмі белгісіз.
Екі теория басым - бұл in vivo ДНҚ-ны қабылдау арнайы емес, ұқсас әдіспен жүреді фаго- немесе пиноцитоз,[21] немесе арнайы рецепторлар арқылы.[57] Олар 30кДа бетін қамтуы мүмкін рецептор, немесе макрофаг рецепторлар. 30kDa беткі рецепторы 4500 а.к. ДНҚ фрагменттерімен арнайы байланысады (содан кейін олар ішкі күйге енеді) және кәсіби APC мен T-жасушаларында кездеседі. Макрофагты жою рецепторлары әртүрлі макромолекулалармен, соның ішінде полиомен байланысадырибонуклеотидтер және осылайша ДНҚ-ны алуға үміткерлер.[57][58] Рецепторлардың көмегімен ДНҚ-ны қабылдаудың болуы жеңілдетуі мүмкін полиганилат тізбегі. Гендік мылтықты жеткізу жүйелері, катиондық липосома қаптамасы және басқа да жеткізу әдістері бұл енгізу әдісін айналып өтеді, бірақ оны түсіну мал шаруашылығында маңызды болуы мүмкін шығындарды азайту үшін пайдалы болуы мүмкін (мысалы, цитофетиндерге деген қажеттілікті азайту арқылы).
Сүйек кемігінен шыққан жасушалар арқылы антигенді ұсыну
Зерттеулер химикалық тышқандар антигеннің дендритті жасушалар, макрофагтар және мамандандырылған құрамына кіретін сүйек кемігінен шыққан жасушалармен ұсынылатындығын көрсетті. В-жасушалар кәсіби деп аталады антигенді ұсынатын жасушалар (APC).[49][59] Теріге гендік мылтық егілгеннен кейін трансфекцияланған Лангерганс жасушалары ағынды суларға көшу лимфа түйіні антигендерді ұсыну.[6] IM және ID инъекцияларынан кейін дендритті жасушалар ағызатын лимфа түйінінде антигенді ұсынады[56] перифериялық қанда және трансфекцияланған макрофагтар табылған.[60]
Дендритті жасушаларды немесе макрофагтарды тікелей трансфекциялаудан басқа, IM, ID және гендік мылтық ДНҚ жеткізілгеннен кейін кросс-приминг пайда болады. Сүйек кемігінен алынған клетка MHC класы аясында басқа жасушада синтезделген ақуыздардан пептидтерді ұсынғанда кросс-приминг пайда болады, бұл Т-жасушаларының цитотоксикалық реакцияларын түзуі мүмкін және толық иммундық жауап үшін маңызды болып көрінеді.[6][61]
Мақсатты сайт рөлі
IM және ID ДНҚ жеткізу иммундық жауаптарды басқаша бастайды. Теріде кератиноциттер, фибробласттар және Лангерганс жасушалары антигендерді қабылдайды және экспрессиялайды және антиденеге алғашқы жауап беру үшін жауап береді. Лангерганстың трансфекцияланған жасушалары теріден (12 сағат ішінде) ағып кететін лимфа түйініне ауысады, сонда олар В- және Т-жасушаларының екінші реттік реакцияларын алады. Қаңқа бұлшықетінде жолақты бұлшықет жасушалары жиі трансфекцияланады, бірақ иммундық жауапта маңызды емес болып көрінеді. Оның орнына, ДНҚ егілген лимфа түйініне бірнеше минут ішінде егіледі, мұнда дистальды дендритті жасушалар трансфекцияланып, иммундық реакцияны бастайды. Трансфекцияланған миоциттер кәсіби БТР сатуға арналған антигеннің «резервуары» ретінде көрінеді.[21][54][61]
Иммундық реакцияны қолдау
ДНҚ-ға қарсы вакцинация антиген-антидене кешендерін көрсету арқылы тиімді иммундық жады қалыптастырады фолликулярлық дендритті жасушалар (FDC), олар В-жасушаларының күшті стимуляторлары болып табылады. Т-жасушаларын ұқсас, герминалды орталық дендритті жасушалар қоздыруы мүмкін. FDC иммундық жадыны қалыптастыра алады, өйткені антиденелер өндірісі антигеннің ұзақ мерзімді экспрессиясымен «қабаттасады», бұл антиген-антидене иммунокомплекстерінің пайда болуына және FDC арқылы көрінуіне мүмкіндік береді.[6]
Интерферондар
Хелпер де, цитотоксикалық Т-жасушалар да интерферондарды бөлу арқылы вирустық инфекцияларды басқара алады. Цитотоксикалық Т жасушалары әдетте вирусты жұқтырған жасушаларды өлтіреді. Алайда, оларды вирусқа қарсы цитокиндерді бөлу үшін ынталандыруға болады IFN-γ және TNF-α, олар жасушаны өлтірмейді, бірақ вирустық компоненттердің экспрессиясын төмендету арқылы вирустық инфекцияны шектейді.[62] ДНҚ-ға қарсы вакцинацияларды вирустық инфекцияларды тежеу үшін IFN-дің көмегімен басқаруға болады. Бұл В гепатитіне қатысты.[63] IFN-γ безгек инфекциясын бақылауда өте маңызды[64] және безгекке қарсы ДНҚ вакциналарын қарастыру болып табылады.
Иммундық жауап модуляциясы
Цитокинді модуляциялау
Тиімді вакцина берілген патогенге сәйкес иммундық жауап тудыруы керек. ДНҚ вакциналары Т-жасушаларының TH1 немесе TH2 профильдеріне қатысты поляризациясы және қажет болған жағдайда CTL және / немесе антидене түзуі мүмкін. Мұны антиген формасына, яғни жасуша ішілік және бөліну түріне, жеткізу әдісі мен дозасына өзгерістер енгізу арқылы жүзеге асыруға болады.[41][42][65][66][67] Мұны иммундық реттеуші молекулаларды, яғни цитокиндерді кодтайтын плазмидті ДНҚ-ны бірлесіп енгізу арқылы да жүзеге асыруға болады. лимфокиндер немесе ко-стимуляторлы молекулалар. Бұл «генетикалық адъюванттар«Келесі түрде басқарылуы мүмкін:
- біреуі иммуногенді, екіншісі цитокинді кодтайтын 2 плазмиданың қоспасы
- бір немесе екі поликистронды вектор, спейсерлік аймақтармен бөлінген
- плазмида-кодталған химеранемесе термоядролық ақуыз
Жалпы алғанда, қабынуға қарсы агенттерді бірге қолдану (мысалы, әртүрлі) интерлейкиндер, ісік некрозының факторы, және GM-CSF) және TH2 индукциялайтын цитокиндер антиденелердің реакциясын күшейтеді, ал қабынуға қарсы агенттер мен TH1 индукциялайтын цитокиндер гуморальды реакцияларды төмендетеді және цитотоксикалық реакцияларды жоғарылатады (вирусты қорғауда маңызды). Сияқты бірлескен ынталандырушы молекулалар B7-1, B7-2 және CD40L кейде қолданылады.
Бұл тұжырымдама pDNA кодтаудың жергілікті әкімшілігінде қолданылды IL-10.[33] В7-1 кодтайтын плазмида (АПК-дағы лиганд) ісік модельдеріндегі иммундық реакцияны ойдағыдай күшейтті. GM-CSF пен циркумспорозоит ақуызын кодтайтын плазмидаларды араластыру P. yoelii (PyCSP) кейінгі қиындықтардан қорғанысты күшейтті (ал тек плазмида-кодталған PyCSP-де олай болмаған). GM-CSF дендритті жасушалардың антигенді тиімдірек көрсетуіне және IL-2 түзілуін және TH жасушаларының белсенділенуін күшейтіп, иммундық жауаптың жоғарылауына себеп болды деген ұсыныс жасалды.[50] Мұны алдымен pPyCSP және pGM-CSF қоспасымен сүрту, содан кейін рекомбинантпен күшейту арқылы жақсартуға болады poxvirus PyCSP білдіретін.[68] Алайда GM-CSF (немесе IFN-γ, немесе IL-2) кодтайтын плазмидалар мен термоядролық ақуызды бірге инъекциялау P. chabaudi мерозоит беткі белогы 1 (C-terminus) -гепатит В вирусының беткі белогы (PcMSP1-HBs) тек pPcMSP1-HBs жеткізумен алынған қорғаумен салыстырғанда, қиындықтардан қорғауды жойды.[30]
Генетикалық адъюванттардың артықшылығы - олардың арзан бағасы және қарапайым әкімшілігі, сонымен қатар тұрақсыздықты болдырмау рекомбинантты цитокиндер және ықтимал уытты, «әдеттегі» адъюванттар (мысалы алюм, кальций фосфаты, монофосфорил липиді А, тырысқақ токсин, катионды және маннанмен жабылған липосомалар, QS21, карбоксиметил целлюлоза және ubenimix).[6][21] Алайда цитокиннің ұзақ экспрессиясының ықтимал уыттылығы анықталмаған. Көптеген коммерциялық маңызды жануарлар түрлерінде цитокин гендері анықталмаған және оқшауланбаған. Сонымен қатар, әртүрлі плазмидтермен кодталған цитокиндер иммундық жүйені жеткізу мерзіміне сәйкес әртүрлі модуляциялайды. Мысалы, кейбір цитокин плазмидасы ДНҚ-лары иммуногенді пДНҚ-дан кейін жақсы жеткізіледі, өйткені алдын-ала немесе бірге жіберу нақты реакцияларды төмендетіп, ерекше емес реакцияларды жоғарылатуы мүмкін.[69]
Иммуностимуляторлы CpG мотивтері
Плазмидті ДНҚ-ның өзі иммундық жүйеге адъювантивті әсер ететін көрінеді.[5][6] Бактериялардан алынған ДНҚ туа біткен иммундық қорғаныс механизмдерін, дендритті жасушалардың активтенуін және TH1 цитокиндерін өндіруді тудыруы мүмкін.[45][70] Бұл иммуностимуляторлы CpG динуклеотидтерінің белгілі бірізділіктерін тануға байланысты.[66][71] CpG стимуляторлық (CpG-S) тізбектері бактериядан шыққан ДНҚ-да эукариоттарға қарағанда жиырма есе жиі кездеседі. Себебі эукариоттар «CpG-дің басылуын» көрсетеді, яғни CpG динуклеотидті жұптар күтілгеннен әлдеқайда сирек кездеседі. Сонымен қатар, CpG-S тізбегі гипометилденеді. Бұл бактериялық ДНҚ-да жиі кездеседі, ал эукариоттарда пайда болатын CpG мотивтері цитозиндік нуклеотидте метилденеді. Керісінше, иммундық реакцияның белсенділігін тежейтін нуклеотидтік тізбектер (CpG нейтралдауы немесе CpG-N деп аталады) эукариоттық геномдарда көп ұсынылған.[72] Оңтайлы иммуностимуляторлық реттілік - бұл екі 5 ’қоршалған метилденбеген CpG динуклеотид. пуриндер және екі 3 ’ пиримидиндер.[66][70] Сонымен қатар, иммуностимулятордан тыс аймақтар гексамер болуы тиіс гуанин-байланысты қамтамасыз ету және мақсатты ұяшықтарға сіңіру.
Туа біткен жүйе адаптивті иммундық жүйемен жұмыс істейді, ДНҚ кодталған ақуызға қарсы реакция жасайды. CpG-S тізбегі B-жасушаларының поликлоналды активтенуін және цитокиннің экспрессиясының және секрециясының реттелуін тудырады.[73] Stimulated macrophages secrete IL-12, IL-18, TNF-α, IFN-α, IFN-β and IFN-γ, while stimulated B-cells secrete IL-6 and some IL-12.[21][73][74]
Manipulation of CpG-S and CpG-N sequences in the plasmid backbone of DNA vaccines can ensure the success of the immune response to the encoded antigen and drive the immune response toward a TH1 phenotype. This is useful if a pathogen requires a TH response for protection. CpG-S sequences have also been used as external adjuvants for both DNA and recombinant protein vaccination with variable success rates. Other organisms with hypomethylated CpG motifs have demonstrated the stimulation of polyclonal B-cell expansion.[дәйексөз қажет] The mechanism behind this may be more complicated than simple methylation – hypomethylated murine DNA has not been found to mount an immune response.
Most of the evidence for immunostimulatory CpG sequences comes from murine studies. Extrapolation of this data to other species requires caution – individual species may require different flanking sequences, as binding specificities of scavenger receptors vary across species. Additionally, species such as ruminants may be insensitive to immunostimulatory sequences due to their large gastrointestinal load.
Alternative boosts
DNA-primed immune responses can be boosted by the administration of recombinant protein or recombinant poxviruses. "Prime-boost" strategies with recombinant protein have successfully increased both neutralising antibody titre, and antibody avidity and persistence, for weak immunogens, such as HIV-1 envelope protein.[6][75] Recombinant virus boosts have been shown to be very efficient at boosting DNA-primed CTL responses. Priming with DNA focuses the immune response on the required immunogen, while boosting with the recombinant virus provides a larger amount of expressed antigen, leading to a large increase in specific CTL responses.
Prime-boost strategies have been successful in inducing protection against malarial challenge in a number of studies. Primed mice with plasmid DNA encoding Plasmodium yoelii circumsporozoite surface protein (PyCSP), then boosted with a recombinant vaccinia virus expressing the same protein had significantly higher levels of antibody, CTL activity and IFN-γ, and hence higher levels of protection, than mice immunized and boosted with plasmid DNA alone.[76] This can be further enhanced by priming with a mixture of plasmids encoding PyCSP and murine GM-CSF, before boosting with recombinant vaccinia virus.[68] An effective prime-boost strategy for the simian malarial model P. knowlesi has also been demonstrated.[77] Rhesus monkeys were primed with a multicomponent, multistage DNA vaccine encoding two liver-stage antigens – the circumsporozoite surface protein (PkCSP) and sporozoite surface protein 2 (PkSSP2) – and two blood stage antigens – the apical merozoite surface protein 1 (PkAMA1) and merozoite surface protein 1 (PkMSP1p42). They were then boosted with a recombinant canarypox virus encoding all four antigens (ALVAC-4). Immunized monkeys developed antibodies against sporozoites and infected erythrocytes, and IFN-γ-secreting T-cell responses against peptides from PkCSP. Partial protection against sporozoite challenge was achieved, and mean parasitemia was significantly reduced, compared to control monkeys. These models, while not ideal for extrapolation to P. falciparum in humans, will be important in pre-clinical trials.
Enhancing immune responses
ДНҚ
The efficiency of DNA immunization can be improved by stabilising DNA against degradation, and increasing the efficiency of delivery of DNA into antigen-presenting cells.[6] This has been demonstrated by coating biodegradable cationic microparticles (such as poly(lactide-co-glycolide) formulated with cetyltrimethylammonium bromide) with DNA. Such DNA-coated microparticles can be as effective at raising CTL as recombinant viruses, especially when mixed with alum. Particles 300 nm in diameter appear to be most efficient for uptake by antigen presenting cells.[6]
Alphavirus vectors
Recombinant alphavirus-based vectors have been used to improve DNA vaccination efficiency.[6] The gene encoding the antigen of interest is inserted into the alphavirus replicon, replacing structural genes but leaving non-structural replicase genes intact. The Sindbis вирусы және Semliki Forest вирусы have been used to build recombinant альфавирус replicons. Unlike conventional DNA vaccinations alphavirus vectors kill transfected cells and are only transiently expressed. Alphavirus replicase genes are expressed in addition to the vaccine insert. It is not clear how alphavirus replicons raise an immune response, but it may be due to the high levels of protein expressed by this vector, replicon-induced cytokine responses, or replicon-induced apoptosis leading to enhanced antigen uptake by dendritic cells.
Сондай-ақ қараңыз
Әдебиеттер тізімі
- ^ Developing Snake antivenom sera by genetic immunization
- ^ DNA immunization as a technology platform for monoclonal antibody induction
- ^ а б Regalado, Antonio (2 August 2016). "The U.S. government has begun testing its first Zika vaccine in humans". MIT Technology Review Magazine. Алынған 2016-08-06.
- ^ а б c г. e f ж сағ мен j к л м n Alarcon JB, Waine GW, McManus DP (1999). "DNA Vaccines: Technology and Application as Anti-parasite and Anti-microbial Agents". Advances in Parasitology Volume 42. Advances in Parasitology. 42. pp. 343–410. дои:10.1016/S0065-308X(08)60152-9. ISBN 9780120317424. PMID 10050276.
- ^ а б c г. e f ж сағ мен j к л м n o б q р с т сен v Robinson HL, Pertmer TM (2000). DNA vaccines for viral infections: basic studies and applications. Advances in Virus Research. 55. pp. 1–74. дои:10.1016/S0065-3527(00)55001-5. ISBN 9780120398553. PMID 11050940.
- ^ White LO, Gibb E, Newham HC, Richardson MD, Warren RC (July 1979). "Comparison of the growth of virulent and attenuated strains of Candida albicans in the kidneys of normal and cortison-treated mice by chitin assay". Mycopathologia. 67 (3): 173–7. дои:10.1007/bf00470753. PMID 384256. S2CID 31914107.
- ^ Paoletti E, Lipinskas BR, Samsonoff C, Mercer S, Panicali D (January 1984). "Construction of live vaccines using genetically engineered poxviruses: biological activity of vaccinia virus recombinants expressing the hepatitis B virus surface antigen and the herpes simplex virus glycoprotein D". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 81 (1): 193–7. Бибкод:1984PNAS...81..193P. дои:10.1073/pnas.81.1.193. PMC 344637. PMID 6320164.
- ^ US Patent 4722848 - Method for immunizing animals with synthetically modified vaccinia virus
- ^ Ulmer, J. B.; Donnelly, J. J.; Parker, S. E.; Rhodes, G. H.; Felgner, P. L.; Dwarki, V. J.; Gromkowski, S. H.; Deck, R. R.; DeWitt, C. M.; Friedman, A.; Et, Al (1993-03-19). "Heterologous protection against influenza by injection of DNA encoding a viral protein". Ғылым. 259 (5102): 1745–1749. дои:10.1126/science.8456302. ISSN 0036-8075. PMID 8456302.
- ^ Chen Y, Wang S, Lu S (February 2014). "DNA Immunization for HIV Vaccine Development". Вакциналар. 2 (1): 138–59. дои:10.3390/vaccines2010138. PMC 4494200. PMID 26344472.
- ^ "Fort Dodge Animal Health Announces Approval of West Nile Virus DNA Vaccine for Horses". PR Newswire. 2005-07-18. Архивтелген түпнұсқа on 2011-05-16. Алынған 2007-11-21.
- ^ "CDC and Fort Dodge Animal Health Achieve First Licensed DNA Vaccine". CDC. 2005-07-18. Архивтелген түпнұсқа on 2007-08-20. Алынған 2007-11-21.
- ^ Developing Snake antivenom sera by genetic immunization
- ^ DNA immunization as a technology platform for monoclonal antibody induction
- ^ а б Sedegah M, Hedstrom R, Hobart P, Hoffman SL (October 1994). "Protection against malaria by immunization with plasmid DNA encoding circumsporozoite protein". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 91 (21): 9866–70. Бибкод:1994PNAS...91.9866S. дои:10.1073/pnas.91.21.9866. JSTOR 2365723. PMC 44918. PMID 7937907.
- ^ Harmon, B. T.; Aly, A. E.; Padegimas, L.; Sesenoglu-Laird, O.; Cooper, M. J.; Waszczak, B. L. (2014). "Intranasal administration of plasmid DNA nanoparticles yields successful transfection and expression of a reporter protein in rat brain". Gene Therapy. 21 (5): 514–521. дои:10.1038/gt.2014.28. PMID 24670994. S2CID 5560134.
- ^ а б Mor G, Klinman DM, Shapiro S, Hagiwara E, Sedegah M, Norman JA, Hoffman SL, Steinberg AD (August 1995). "Complexity of the cytokine and antibody response elicited by immunizing mice with Plasmodium yoelii circumsporozoite protein plasmid DNA". Journal of Immunology. 155 (4): 2039–46. PMID 7636255.
- ^ Leitner WW, Seguin MC, Ballou WR, Seitz JP, Schultz AM, Sheehy MJ, Lyon JA (December 1997). "Immune responses induced by intramuscular or gene gun injection of protective deoxyribonucleic acid vaccines that express the circumsporozoite protein from Plasmodium berghei malaria parasites". Journal of Immunology. 159 (12): 6112–9. PMID 9550412.
- ^ Böhm W, Kuhröber A, Paier T, Mertens T, Reimann J, Schirmbeck R (June 1996). "DNA vector constructs that prime hepatitis B surface antigen-specific cytotoxic T lymphocyte and antibody responses in mice after intramuscular injection". Journal of Immunological Methods. 193 (1): 29–40. дои:10.1016/0022-1759(96)00035-X. PMID 8690928.
- ^ а б c г. e f ж сағ мен j к Lewis PJ, Babiuk LA (1999). DNA vaccines: a review. Advances in Virus Research. 54. Академиялық баспасөз. pp. 129–88. дои:10.1016/S0065-3527(08)60367-X. ISBN 978-0-12-039854-6. PMID 10547676.
- ^ André S, Seed B, Eberle J, Schraut W, Bültmann A, Haas J (February 1998). "Increased immune response elicited by DNA vaccination with a synthetic gp120 sequence with optimized codon usage". Journal of Virology. 72 (2): 1497–503. дои:10.1128/JVI.72.2.1497-1503.1998. PMC 124631. PMID 9445053.
- ^ Muthumani K, Zhang D, Dayes NS, Hwang DS, Calarota SA, Choo AY, Boyer JD, Weiner DB (September 2003). "Novel engineered HIV-1 East African Clade-A gp160 plasmid construct induces strong humoral and cell-mediated immune responses in vivo". Вирусология. 314 (1): 134–46. дои:10.1016/S0042-6822(03)00459-8. PMID 14517067.
- ^ Oliveira PH, Prather KJ, Prazeres DM, Monteiro GA (September 2009). "Structural instability of plasmid biopharmaceuticals: challenges and implications". Trends in Biotechnology. 27 (9): 503–11. дои:10.1016/j.tibtech.2009.06.004. PMID 19656584.
- ^ Oliveira PH, Mairhofer J (September 2013). "Marker-free plasmids for biotechnological applications - implications and perspectives". Trends in Biotechnology. 31 (9): 539–47. дои:10.1016/j.tibtech.2013.06.001. PMID 23830144.
- ^ Kutzler MA, Weiner DB (October 2008). "DNA vaccines: ready for prime time?". Nature Reviews. Генетика. 9 (10): 776–88. дои:10.1038/nrg2432. PMC 4317294. PMID 18781156.
- ^ Rodriguez F, Zhang J, Whitton JL (November 1997). "DNA immunization: ubiquitination of a viral protein enhances cytotoxic T-lymphocyte induction and antiviral protection but abrogates antibody induction". Journal of Virology. 71 (11): 8497–503. дои:10.1128/JVI.71.11.8497-8503.1997. PMC 192313. PMID 9343207.
- ^ а б Tobery TW, Siliciano RF (March 1997). "Targeting of HIV-1 antigens for rapid intracellular degradation enhances cytotoxic T lymphocyte (CTL) recognition and the induction of de novo CTL responses in vivo after immunization". The Journal of Experimental Medicine. 185 (5): 909–20. дои:10.1084/jem.185.5.909. PMC 2196169. PMID 9120397.
- ^ Huebener N, Fest S, Strandsby A, Michalsky E, Preissner R, Zeng Y, Gaedicke G, Lode HN (July 2008). "A rationally designed tyrosine hydroxylase DNA vaccine induces specific antineuroblastoma immunity". Molecular Cancer Therapeutics. 7 (7): 2241–51. дои:10.1158/1535-7163.MCT-08-0109. PMID 18645033.
- ^ а б Wunderlich G, Moura IC, del Portillo HA (October 2000). "Genetic immunization of BALB/c mice with a plasmid bearing the gene coding for a hybrid merozoite surface protein 1-hepatitis B virus surface protein fusion protects mice against lethal Plasmodium chabaudi chabaudi PC1 infection". Infection and Immunity. 68 (10): 5839–45. дои:10.1128/IAI.68.10.5839-5845.2000. PMC 101545. PMID 10992493.
- ^ Weiner DB, Kennedy RC (1999). "Genetic vaccines". Ғылыми американдық. 281 (1): 34–41. Бибкод:1999SciAm.281a..50W. дои:10.1038/scientificamerican0799-50. PMID 10396782. Архивтелген түпнұсқа 2009-03-25. Алынған 2007-11-21.
- ^ Widera G, Austin M, Rabussay D, Goldbeck C, Barnett SW, Chen M, Leung L, Otten GR, Thudium K, Selby MJ, Ulmer JB (May 2000). "Increased DNA vaccine delivery and immunogenicity by electroporation in vivo". Journal of Immunology. 164 (9): 4635–40. дои:10.4049/jimmunol.164.9.4635. PMID 10779767.
- ^ а б Daheshia M, Kuklin N, Kanangat S, Manickan E, Rouse BT (August 1997). "Suppression of ongoing ocular inflammatory disease by topical administration of plasmid DNA encoding IL-10". Journal of Immunology. 159 (4): 1945–52. PMID 9257860.
- ^ а б Chen Y, Webster RG, Woodland DL (March 1998). "Induction of CD8+ T cell responses to dominant and subdominant epitopes and protective immunity to Sendai virus infection by DNA vaccination". Journal of Immunology. 160 (5): 2425–32. PMID 9498786.
- ^ Lode HN, Huebener N, Zeng Y, Fest S, Weixler S, Gaedicke G (December 2004). "DNA minigene vaccination for adjuvant neuroblastoma therapy". Нью-Йорк Ғылым академиясының жылнамалары. 1028 (1): 113–21. Бибкод:2004NYASA1028..113L. дои:10.1196/annals.1322.012. PMID 15650237. S2CID 27240738.
- ^ Sizemore DR, Branstrom AA, Sadoff JC (October 1995). "Attenuated Shigella as a DNA delivery vehicle for DNA-mediated immunization". Ғылым. 270 (5234): 299–302. Бибкод:1995Sci...270..299S. дои:10.1126/science.270.5234.299. PMID 7569980. S2CID 12532901.
- ^ Nealon, Cory (25 November 2014). "A hybrid vehicle that delivers DNA". The State University of New York at Buffalo. Алынған 16 желтоқсан 2014.
- ^ Jones CH, et al. (August 2014). "Hybrid biosynthetic gene therapy vector development and dual engineering capacity". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 111 (34): 12360–5. Бибкод:2014PNAS..11112360J. дои:10.1073/pnas.1411355111. PMC 4151754. PMID 25114239.
- ^ Barry MA, Lai WC, Johnston SA (October 1995). "Protection against mycoplasma infection using expression-library immunization". Табиғат. 377 (6550): 632–5. Бибкод:1995Natur.377..632B. дои:10.1038/377632a0. PMID 7566175. S2CID 4306972.
- ^ Fynan EF, Webster RG, Fuller DH, Haynes JR, Santoro JC, Robinson HL (December 1993). "DNA vaccines: protective immunizations by parenteral, mucosal, and gene-gun inoculations". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 90 (24): 11478–82. Бибкод:1993PNAS...9011478F. дои:10.1073/pnas.90.24.11478. PMC 48007. PMID 8265577.
- ^ а б c г. e Feltquate DM, Heaney S, Webster RG, Robinson HL (March 1997). "Different T helper cell types and antibody isotypes generated by saline and gene gun DNA immunization". Journal of Immunology. 158 (5): 2278–84. PMID 9036975.
- ^ а б c г. Boyle CM, Morin M, Webster RG, Robinson HL (December 1996). "Role of different lymphoid tissues in the initiation and maintenance of DNA-raised antibody responses to the influenza virus H1 glycoprotein". Journal of Virology. 70 (12): 9074–8. дои:10.1128/JVI.70.12.9074-9078.1996. PMC 191015. PMID 8971047.
- ^ Sällberg M, Townsend K, Chen M, O'Dea J, Banks T, Jolly DJ, Chang SM, Lee WT, Milich DR (July 1997). "Characterization of humoral and CD4+ cellular responses after genetic immunization with retroviral vectors expressing different forms of the hepatitis B virus core and e antigens". Journal of Virology. 71 (7): 5295–303. дои:10.1128/JVI.71.7.5295-5303.1997. PMC 191766. PMID 9188598.
- ^ Banchereau J, Steinman RM (March 1998). "Dendritic cells and the control of immunity". Табиғат. 392 (6673): 245–52. Бибкод:1998Natur.392..245B. дои:10.1038/32588. PMID 9521319. S2CID 4388748.
- ^ а б Jakob T, Walker PS, Krieg AM, Udey MC, Vogel JC (September 1998). "Activation of cutaneous dendritic cells by CpG-containing oligodeoxynucleotides: a role for dendritic cells in the augmentation of Th1 responses by immunostimulatory DNA". Journal of Immunology. 161 (6): 3042–9. PMID 9743369.
- ^ а б Raz E, Tighe H, Sato Y, Corr M, Dudler JA, Roman M, Swain SL, Spiegelberg HL, Carson DA (May 1996). "Preferential induction of a Th1 immune response and inhibition of specific IgE antibody formation by plasmid DNA immunization". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 93 (10): 5141–5. Бибкод:1996PNAS...93.5141R. дои:10.1073/pnas.93.10.5141. PMC 39421. PMID 8643542.
- ^ а б Fu TM, Friedman A, Ulmer JB, Liu MA, Donnelly JJ (April 1997). "Protective cellular immunity: cytotoxic T-lymphocyte responses against dominant and recessive epitopes of influenza virus nucleoprotein induced by DNA immunization". Journal of Virology. 71 (4): 2715–21. дои:10.1128/JVI.71.4.2715-2721.1997. PMC 191393. PMID 9060624.
- ^ а б c Restifo NP, Bacík I, Irvine KR, Yewdell JW, McCabe BJ, Anderson RW, Eisenlohr LC, Rosenberg SA, Bennink JR (May 1995). "Antigen processing in vivo and the elicitation of primary CTL responses". Journal of Immunology. 154 (9): 4414–22. PMC 1952186. PMID 7722298.
- ^ а б c Iwasaki A, Stiernholm BJ, Chan AK, Berinstein NL, Barber BH (May 1997). "Enhanced CTL responses mediated by plasmid DNA immunogens encoding costimulatory molecules and cytokines". Journal of Immunology. 158 (10): 4591–601. PMID 9144471.
- ^ а б Weiss WR, Ishii KJ, Hedstrom RC, Sedegah M, Ichino M, Barnhart K, Klinman DM, Hoffman SL (September 1998). "A plasmid encoding murine granulocyte-macrophage colony-stimulating factor increases protection conferred by a malaria DNA vaccine". Journal of Immunology. 161 (5): 2325–32. PMID 9725227.
- ^ Tsuji T, Hamajima K, Fukushima J, Xin KQ, Ishii N, Aoki I, Ishigatsubo Y, Tani K, et al. (April 1997). "Enhancement of cell-mediated immunity against HIV-1 induced by coinnoculation of plasmid-encoded HIV-1 antigen with plasmid expressing IL-12". Journal of Immunology. 158 (8): 4008–13. PMID 9103472.
- ^ а б Justewicz DM, Webster RG (October 1996). "Long-term maintenance of B cell immunity to influenza virus hemagglutinin in mice following DNA-based immunization". Вирусология. 224 (1): 10–7. дои:10.1006/viro.1996.0501. PMID 8862394.
- ^ Mancini-Bourgine M, Fontaine H, Bréchot C, Pol S, Michel ML (May 2006). "Immunogenicity of a hepatitis B DNA vaccine administered to chronic HBV carriers". Вакцина. 24 (21): 4482–9. дои:10.1016/j.vaccine.2005.08.013. PMID 16310901.
- ^ а б Wolff JA, Dowty ME, Jiao S, Repetto G, Berg RK, Ludtke JJ, Williams P, Slautterback DB (December 1992). "Expression of naked plasmids by cultured myotubes and entry of plasmids into T tubules and caveolae of mammalian skeletal muscle". Journal of Cell Science. 103. 103 ( Pt 4) (4): 1249–59. PMID 1487500.
- ^ Anderson RG, Kamen BA, Rothberg KG, Lacey SW (January 1992). "Potocytosis: sequestration and transport of small molecules by caveolae". Ғылым. 255 (5043): 410–1. Бибкод:1992Sci...255..410A. дои:10.1126/science.1310359. PMID 1310359.
- ^ а б Casares S, Inaba K, Brumeanu TD, Steinman RM, Bona CA (November 1997). "Antigen presentation by dendritic cells after immunization with DNA encoding a major histocompatibility complex class II-restricted viral epitope". The Journal of Experimental Medicine. 186 (9): 1481–6. дои:10.1084/jem.186.9.1481. PMC 2199124. PMID 9348305.
- ^ а б Bennett RM, Gabor GT, Merritt MM (December 1985). "DNA binding to human leukocytes. Evidence for a receptor-mediated association, internalization, and degradation of DNA". The Journal of Clinical Investigation. 76 (6): 2182–90. дои:10.1172/JCI112226. PMC 424340. PMID 3001145.
- ^ Bennet RM, Hefeneider SH, Bakke A, Merritt M, Smith CA, Mourich D, Heinrich MC (May 1988). "The production and characterization of murine monoclonal antibodies to a DNA receptor on human leukocytes". Journal of Immunology. 140 (9): 2937–42. PMID 2452195.
- ^ Corr M, Lee DJ, Carson DA, Tighe H (October 1996). "Gene vaccination with naked plasmid DNA: mechanism of CTL priming". The Journal of Experimental Medicine. 184 (4): 1555–60. дои:10.1084/jem.184.4.1555. PMC 2192808. PMID 8879229.
- ^ Chattergoon MA, Robinson TM, Boyer JD, Weiner DB (June 1998). "Specific immune induction following DNA-based immunization through in vivo transfection and activation of macrophages/antigen-presenting cells". Journal of Immunology. 160 (12): 5707–18. PMID 9637479.
- ^ а б Torres CA, Iwasaki A, Barber BH, Robinson HL (May 1997). "Differential dependence on target site tissue for gene gun and intramuscular DNA immunizations". Journal of Immunology. 158 (10): 4529–32. PMID 9144463.
- ^ Franco A, Guidotti LG, Hobbs MV, Pasquetto V, Chisari FV (August 1997). "Pathogenetic effector function of CD4-positive T helper 1 cells in hepatitis B virus transgenic mice". Journal of Immunology. 159 (4): 2001–8. PMID 9257867.
- ^ Mancini M, Hadchouel M, Davis HL, Whalen RG, Tiollais P, Michel ML (October 1996). "DNA-mediated immunization in a transgenic mouse model of the hepatitis B surface antigen chronic carrier state". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 93 (22): 12496–501. Бибкод:1996PNAS...9312496M. дои:10.1073/pnas.93.22.12496. PMC 38020. PMID 8901610.
- ^ Doolan DL, Hoffman SL (July 1999). "IL-12 and NK cells are required for antigen-specific adaptive immunity against malaria initiated by CD8+ T cells in the Plasmodium yoelii model". Journal of Immunology. 163 (2): 884–92. PMID 10395683.
- ^ Cardoso AI, Blixenkrone-Moller M, Fayolle J, Liu M, Buckland R, Wild TF (November 1996). "Immunization with plasmid DNA encoding for the measles virus hemagglutinin and nucleoprotein leads to humoral and cell-mediated immunity". Вирусология. 225 (2): 293–9. дои:10.1006/viro.1996.0603. PMID 8918915.
- ^ а б c Sato Y, Roman M, Tighe H, Lee D, Corr M, Nguyen MD, Silverman GJ, Lotz M, Carson DA, Raz E (July 1996). "Immunostimulatory DNA sequences necessary for effective intradermal gene immunization". Ғылым. 273 (5273): 352–4. Бибкод:1996Sci...273..352S. дои:10.1126/science.273.5273.352. PMID 8662521. S2CID 9333197.
- ^ Weiss R, Leitner WW, Scheiblhofer S, Chen D, Bernhaupt A, Mostböck S, Thalhamer J, Lyon JA (October 2000). "Genetic vaccination against malaria infection by intradermal and epidermal injections of a plasmid containing the gene encoding the Plasmodium berghei circumsporozoite protein". Infection and Immunity. 68 (10): 5914–9. дои:10.1128/IAI.68.10.5914-5919.2000. PMC 101554. PMID 10992502.
- ^ а б Sedegah M, Weiss W, Sacci JB, Charoenvit Y, Hedstrom R, Gowda K, Majam VF, Tine J, Kumar S, Hobart P, Hoffman SL (June 2000). "Improving protective immunity induced by DNA-based immunization: priming with antigen and GM-CSF-encoding plasmid DNA and boosting with antigen-expressing recombinant poxvirus". Journal of Immunology. 164 (11): 5905–12. дои:10.4049/jimmunol.164.11.5905. PMID 10820272.
- ^ Barouch DH, Santra S, Steenbeke TD, Zheng XX, Perry HC, Davies ME, Freed DC, Craiu A, Strom TB, Shiver JW, Letvin NL (August 1998). "Augmentation and suppression of immune responses to an HIV-1 DNA vaccine by plasmid cytokine/Ig administration". Journal of Immunology. 161 (4): 1875–82. PMID 9712056.
- ^ а б Krieg AM, Yi AK, Matson S, Waldschmidt TJ, Bishop GA, Teasdale R, Koretzky GA, Klinman DM (April 1995). "CpG motifs in bacterial DNA trigger direct B-cell activation". Табиғат. 374 (6522): 546–9. Бибкод:1995Natur.374..546K. дои:10.1038/374546a0. PMID 7700380. S2CID 4261304.
- ^ Klinman DM, Yamshchikov G, Ishigatsubo Y (April 1997). "Contribution of CpG motifs to the immunogenicity of DNA vaccines". Journal of Immunology. 158 (8): 3635–9. PMID 9103425.
- ^ Krieg AM, Wu T, Weeratna R, Efler SM, Love-Homan L, Yang L, Yi AK, Short D, Davis HL (October 1998). "Sequence motifs in adenoviral DNA block immune activation by stimulatory CpG motifs". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 95 (21): 12631–6. Бибкод:1998PNAS...9512631K. дои:10.1073/pnas.95.21.12631. PMC 22882. PMID 9770537.
- ^ а б Klinman DM, Yi AK, Beaucage SL, Conover J, Krieg AM (April 1996). "CpG motifs present in bacteria DNA rapidly induce lymphocytes to secrete interleukin 6, interleukin 12, and interferon gamma". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 93 (7): 2879–83. Бибкод:1996PNAS...93.2879K. дои:10.1073/pnas.93.7.2879. PMC 39727. PMID 8610135.
- ^ Yi AK, Chace JH, Cowdery JS, Krieg AM (January 1996). "IFN-gamma promotes IL-6 and IgM secretion in response to CpG motifs in bacterial DNA and oligodeoxynucleotides". Journal of Immunology. 156 (2): 558–64. PMID 8543806.
- ^ Letvin NL, Montefiori DC, Yasutomi Y, Perry HC, Davies ME, Lekutis C, Alroy M, Freed DC, Lord CI, Handt LK, Liu MA, Shiver JW (August 1997). "Potent, protective anti-HIV immune responses generated by bimodal HIV envelope DNA plus protein vaccination". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 94 (17): 9378–83. Бибкод:1997PNAS...94.9378L. дои:10.1073/pnas.94.17.9378. PMC 23198. PMID 9256490.
- ^ Sedegah M, Jones TR, Kaur M, Hedstrom R, Hobart P, Tine JA, Hoffman SL (June 1998). "Boosting with recombinant vaccinia increases immunogenicity and protective efficacy of malaria DNA vaccine". Америка Құрама Штаттарының Ұлттық Ғылым Академиясының еңбектері. 95 (13): 7648–53. Бибкод:1998PNAS...95.7648S. дои:10.1073/pnas.95.13.7648. PMC 22711. PMID 9636204.
- ^ Rogers WO, Baird JK, Kumar A, Tine JA, Weiss W, Aguiar JC, Gowda K, Gwadz R, Kumar S, Gold M, Hoffman SL (September 2001). "Multistage multiantigen heterologous prime boost vaccine for Plasmodium knowlesi malaria provides partial protection in rhesus macaques". Infection and Immunity. 69 (9): 5565–72. дои:10.1128/IAI.69.9.5565-5572.2001. PMC 98670. PMID 11500430.
Әрі қарай оқу
| Шолия has a profile for ДНҚ вакцинасы (Q578537). |
- Hooper JW, Thompson E, Wilhelmsen C, Zimmerman M, Ichou MA, Steffen SE, Schmaljohn CS, Schmaljohn AL, Jahrling PB (May 2004). "Smallpox DNA vaccine protects nonhuman primates against lethal monkeypox". Journal of Virology. 78 (9): 4433–43. дои:10.1128/JVI.78.9.4433-4443.2004. PMC 387704. PMID 15078924.